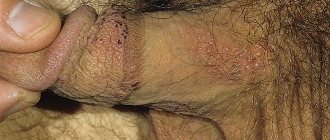
В последние годы увеличивается заболеваемость папилломавирусной инфекцией. По данным ВОЗ, ежегодно в мире около 250 000 женщин с ВПЧ-инфекцией умирает от рака шейки матки. На этом фоне поиск эффективных методов лечения этой инфекции становится чрезвычайно важным. Проблема ее диагностики и лечения привлекает внимание врачей различных специальностей: дерматологов, гинекологов, урологов, онкологов, иммунологов, вирусологов, патоморфологов. На данный момент большинство ученых пришли к единому мнению – с проявлениями вируса папилломы человека можно бороться при помощи применения иммуномодуляторов с противовирусной активностью.
- Что такое иммуномодуляторы
- Список препаратов
- Противовирусные при ВПЧ
- Можно ли применять ВИФЕРОН Свечи вагинально?
- Лечение слизистой у мужчин
- Альтернативные методы лечения
Что такое иммуномодуляторы
К иммуномодулирующим средствам относятся препараты химической и биологической природы, способные модулировать (угнетать или стимулировать) реакции иммунитета. При этом иммунологический эффект иммуномодуляторов зависит от исходного состояния иммунитета человека: эти лекарственные средства понижают повышенные и повышают пониженные показатели иммунитета. Особенно данный постулат относится к препаратам интерферона. К иммунотерапии также относятся методы лечения, основанные на использовании иммунотропных средств при заболеваниях, в патогенезе которых имеются нарушения, затрагивающие систему иммунитета.
Основной критерий для назначения иммуномодуляторов – это клиническая картина заболевания (острого или хронического инфекционно-воспалительного процесса), который сопровождается снижением параметров иммунитета и трудно поддается лечению. В этом случае иммуномодуляторы играют роль главного помощника, который способствует эффективной терапии и избавляет от проявлений многих заболеваний.
Поскольку ВПЧ-инфекция тоже относится к недугам, с которыми достаточно непросто бороться, а исход лечения зависит от состояния иммунитета, при лечении этой инфекции широко применяют различные иммуномодуляторы.
Для чего назначают иммуномодуляторы при папилломавирусной инфекции
Слабый иммунитет – это основная причина «пробуждения» ВПЧ. Поэтому при противовирусной терапии больший упор врачи делают именно на те препараты, которые стимулируют активность иммунной системы и укрепляют ее. К таким препарат относятся различные формы иммуномодуляторов: как химических, так и натуральных.
Естественно, что при помощи этих средств нельзя излечить заболевание полностью и очистить кровь от вируса, поэтому иммуномодуляторы следует принимать в комплексе с:
- оперативным удалением доброкачественных образований, если они проявили себя;
- профилактическими мерами, предупреждающими рецидивы;
- постлечебным наблюдением больного.
Иммуномодуляторы при ВПЧ: список препаратов
Препараты, которые являются синтетическими комплексными производными пурина
Эта группа иммуномодуляторов, применяющихся при лечении проявлений вируса папилломы человека, обладают иммуностимулирующей активностью и неспецифическим противовирусным действием. Они восстанавливают активность лимфоцитов, которые являются главными клетками иммунной системы. Клинически доказано, что именно низкая активность лимфоцитов является предрасполагающим фактором к яркому развитию клинических проявлений ВПЧ. Также этот вид препаратов повышает функционирование натуральных киллеров и так называемыхТ-хелперов – T-лимфоцитов, главной функцией которых является координация иммунного ответа.
Некоторые из препаратов этой группы имеют обширный список побочных действий, включающих проблемы с работой ЖКТ, печени и желчевыводящих путей. Также возможны побочные реакции в виде головной боли, сонливости, бессонницы, зуда и болей в суставах. Среди противопоказаний – детский возраст до 3 лет, беременность, заболевания почек и повышенная чувствительность к компонентам препарата.
Препараты с действующим веществом глюкозаминилмурамилдипептид (ГМДП)
ГМДП – это фрагмент оболочки патогенных бактерий, вызывающих инфекционно-воспалительные заболевания различных органов и систем. При попадании этого фрагмента в организм иммунная система воспринимает его как чужеродный патогенный агент и сразу же начинает выработку антител. Благодаря этому происходит общая активация всей иммунной системы, что способствует выздоровлению или же снижению частоты рецидивов вирусных инфекций, в том числе ВПЧ.
Среди побочных эффектов – повышение температуры тела до субфебрильных и фебрильных значений, также возможна диарея. Препараты этой группы противопоказаны при нарушениях обмена веществ и женщинам в период беременности и грудного вскармливания.
Препараты, содержащие в качестве активных компонентов натуральное растительное сырье
Эта группа препаратов была создана на основе открытия лауреата Нобелевской премии Н.Н. Семенова о мощных иммуностимулирующих свойствах биологически активных веществ, содержащихся в клетках растений. Экстракты из растений и вспомогательные компоненты усиливают неспецифическое звено иммунитета, что повышает устойчивость организма человека к различным вирусным и некоторым бактериальным инфекциям. Иммуномодулирующий эффект активизирует лейкоциты, что особенно важно при борьбе с хроническими и затяжными воспалительными процессами.
При применении этих препаратов возможны аллергические реакции. Среди противопоказаний к применению – заболевания выделительной системы, беременность, период лактации и детский возраст до 18 лет.
Местные противовирусные средства растительного происхождения
Аммония глицирризинат
Активный компонент препарата — активированную глицирризиновую кислоту — получают из корня солодки. Оказывает комплексное иммуностимулирующее, противовирусное, противовоспалительное, противозудное действие. Глицирризиновая кислота прерывает репликацию ряда ДНК и РНК вирусов, в том числе вируса простого герпеса, папилломы человека, цитомегаловируса [5].
Показана в качестве препарата для лечения папилломавирусной инфекции и вируса простого герпеса, в том числе и при инфицировании вирусами онкогенного типа. Выпускается в форме спрея, который распыляют на слизистые оболочки и пораженные участки кожи.
Отпуск: без рецепта.
+
Имеет широкий спектр показаний, среди которых профилактика и лечение кандидозного вульвовагинита, дискомфорт в области половых органов. Может применяться при беременности и кормлении грудью; хорошо переносится.
Подофиллотоксин
Активный компонент подофиллина, производного растительных экстрактов, выделяемых из корневищ с корнями подофилла щитовидного — растения семейства барбарисовых. Обладает выраженными противоопухолевыми и противовирусными свойствами, оказывает цитотоксическое действие. При наружном применении прижигает и мумифицирует кондиломы. Применяется в качестве препарата для местного лечения от вируса папилломы человека. Выпускается в форме раствора для обработки остроконечных кондилом [8].
Отпуск: по рецепту.
+
Доказанный эффект. По данным исследований, 0,5 %-ный раствор подофиллотоксина уменьшает число аногенитальных бородавок с 6,3 до 1,1, разрушая около 70 % образований [8].
!
Необходимо соблюдать осторожность при применении — попадание на здоровую кожу может приводить к изъязвлению. Местные реакции при применении, аллергические реакции. Первостольник, отпуская этот противовирусный препарат от папиллом и кондилом, должен обратить внимание клиента на эту особенность и напомнить, что ЛС следует хранить в недоступном для детей месте.
Тетрагидроксиглюкопиранозилксантен
Российский препарат. Активный компонент выделяют из растения копеечника альпийского или копеечника желтеющего.
Согласно инструкции, обладает противовирусной активностью в отношении ВПГ-1 и ВПГ-2, а также цитомегаловируса и некоторых других ДНК-содержащих вирусов. Кроме того, предположительно, препарат активирует клеточный и гуморальный иммунитет, ингибирует рост ряда бактерий и патогенных простейших, в том числе трихомонад, а также оказывает умеренное противовоспалительное действие. Применяют в форме мази в составе комбинированного лечения острых и рецидивирующих форм герпеса, в том числе генитального [5].
Отпуск: без рецепта.
+
Благоприятный профиль безопасности, возможность применять в составе комплексного лечения.
Полисахариды побегов Solanum tuberosum
Рецептурный российский препарат, активный компонент получают из побегов паслена клубненосного. По данным инструкции, проявляет противовирусный эффект в отношении ВПГ-1 и ВПГ-2, способствует индукции интерферонов и повышает иммунный ответ [5]. Следует заметить, что фармакокинетические свойства препарата не изучались. Вагинальные суппозитории применяются в комплексной терапии генитального герпеса.
Отпуск: без рецепта.
+
Высокий профиль безопасности. Побочные эффекты проявляются редко.
Десмодиума канадского травы экстракт
Противовирусный препарат от герпеса растительного происхождения, созданный из сухого экстракта травы десмодиума канадского. По данным инструкции, проявляет противовирусную активность в отношении вирусов герпеса, стимулирует выработку интерферона [5]. Мазь показана для применения при острых и рецидивирующих формах герпеса, в том числе урогенитального.
Отпуск: без рецепта.
+
Высокий профиль безопасности — побочные эффекты не выявлены.
Гипорамина экстракт
Российская разработка на основе экстракта листьев облепихи. По данным инструкции, активен в отношении вирусов простого герпеса, цитомегаловирусов и некоторых других [5]. Мазь, содержащая экстракт гипорамин, показана для лечения и профилактики эпизодов герпеса, в том числе и генитального.
Отпуск: без рецепта.
+
Высокий профиль безопасности; возможность использовать во время беременности и лактации (после консультации с врачом).
Противовирусные препараты против ВПЧ
После заражения клетки вирус может пребывать в свободном виде или проникает в геном клетки. В любом случае вирус изменяет нормальные клеточные процессы. И вместо того, чтобы производить все необходимое для своей жизнедеятельности, клетка обеспечивает механизмы синтеза вирусных молекул ДНК, которые в дальнейшем будут использоваться для создания новых вирусных частиц. Но не всегда вирусы способны вызывать заболевание. При адекватном иммунном ответе организм самостоятельно избавляется от вируса. При неэффективном иммунном ответе организма возможно долгое носительство вируса, что может привести к доброкачественным или злокачественным, в зависимости от типа вируса, проявлениям болезни.
Чтобы разорвать цепь бесконечного размножения вируса и последующего развития заболевания, признана необходимость лечения ВПЧ-инфекции иммуномодуляторами с противовирусной активностью, т.к. на сегодняшний день не разработано ни одного противовирусного от ВПЧ, действующего прицельно на вирус папилломы человека.
ВИФЕРОН при ВПЧ
Существуют ли препараты, которые борются с вирусами и одновременно способствуют восстановлению иммунной системы? Безусловно, такие препараты есть. Одним из таких препаратов, способствующих восстановлению иммунной системы и обладающих широким спектром противовирусной активности, является препарат ВИФЕРОН.
Рекомбинантный интерферон альфа-2b, который входит в состав этого препарата, препятствует синтезу вирусных ДНК и блокирует размножение вируса, способствует восстановлению иммунной системы, а также обладает антипролиферативными свойствами. Он идентичен человеческому интерферону альфа-2b, но производится с помощью современных технологий без использования донорской крови.
Препарат, который выпускается в виде свечей, геля и мази, разработан в результате фундаментальных исследований в области иммунологии, доказавших, что в присутствии антиоксидантов (витамины С, Е) усиливается противовирусное действие интерферона.
Способ применения и дозировки свечей ВИФЕРОН при ВПЧ
ВИФЕРОН Свечи производятся в виде ректальных суппозиториев пулевидной формы бело-желтого или желтого цвета. В процессе лечения препарат подавляет активность вирусов и повышает эффективность собственного иммунного ответа организма на патогенные микроорганизмы.
Препарат в виде Свечей (суппозиториев) можно применять при беременности (с 14-й недели), а также в период грудного вскармливания и при лечении детей.
Рекомендуемая доза для взрослых – ВИФЕРОН 500 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5-10 суток. По клиническим показаниям терапия может быть продолжена.
Беременным со II триместра беременности (начиная с 14-й недели гестации) назначают ВИФЕРОН 500 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 10 суток, затем в течение 9 дней 3 раза с интервалом в 3 дня (на четвертый день) по 1 суппозиторию 2 раза/сут через 12 ч.. Далее каждые 4 недели до родоразрешения – препарат в дозировке 150 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5 суток. При необходимости назначают перед родоразрешением (с 38-й недели гестации) препарат в дозировке 500000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 10 суток.
Поиск путей решения проблемы широкого распространения ВПЧ-инфекции – важнейшая медико-социальная проблема современного здравоохранения. Низкая сексуальная культура населения, частая смена половых партнеров, незащищенный секс увеличивают риск развития ВПЧ-инфекции, способствуя росту числа воспалительных заболеваний генитального тракта, нарушению репродуктивной функции, а также формированию цервикальной интра-эпителиальной неоплазии шейки матки [1, 2].
Ряд штаммов папилломавируса человека высокоонкогенный: в 70% случаев штаммы 16 и 18 ассоциированы с раком шейки матки (РШМ), в 10% – штаммы 31 и 45 [1]. В исследованиях Международного агентства по изучению рака, включивших 3085 случаев инвазивного цервикального рака, ВПЧ-16 был выявлен в 54% случаев сквамозноклеточных карцином и в 42% – аденокарцином, а ВПЧ-18 – в 11 и 37% случаев соответственно [2–4].
Большинство мужчин и женщин, ведущих половую жизнь, инфицируются ВПЧ, при этом главной особенностью данной инфекции считают ее широкое распространение среди подростков и молодых женщин преимущественно до 25 лет. Более чем у 80% женщин ВПЧ диагностируют уже через 2 года после начала половой жизни, при этом при наличии одного полового партнера вирусом заражаются до 20% [2]. ВПЧ обнаруживают у 99,7% женщин с гистологически подтвержденным диагнозом РШМ. Риск инфицированности одним штаммом ВПЧ не снижает риска инфицированности филогенетически родственным типом вируса [3].
По данным современных исследований, 85% женщин с типичными кондиломами вульвы и промежности имеют дополнительные очаги папилломавирусной инфекции во влагалище или на шейке матки, в 10–25% случаев ассоциированные с цервикальными интраэпителиальными неоплазиями (CIN – Cervical intraepithelial neoplasia) различных степеней тяжести [5].
Зачастую папилломавирусная инфекция выявляется совместно с другими заболеваниями, передающимися половым путем: урогенитальным хламидиозом, микоплазмозом, цитомегаловирусной и герпетической инфекциями, что оказывает заметное влияние на клинические проявления, особенности течения и прогноз.
С ВПЧ ассоциированы такие заболевания урогенитального тракта, как хронический эндоцервицит и вагинит, кондиломы шейки матки и наружных половых органов, CIN, РМШ, внутриэпителиальные неоплазии вульвы (VIN – Vulvar Intraepithelial Neoplasia) и вагины (VaIN – Vaginal intraepithelial neoplasia), простатическая интраэпителиальная неоплазия (PIN – Prostate intraepithelial neoplasia) и анальная интраэпителиальная неоплазия (AIN – Anal intraepithelial neoplasia) [6].
Длительное персистирование ВПЧ сопровождается развитием вторичных иммунодефицитных состояний, обусловленных истощением и как следствие недостаточной работой звеньев иммунной системы. На сегодняшний день установлено, что ВПЧ не инфицируют антигенпредставляющие клетки, и является причиной отсутствия прямого пути активации системы иммунитета при данной патологии. Ранние вирусные белки ВПЧ локализуются преимущественно в ядрах инфицированных клеток, не приводя к формированию полноценного иммунного ответа [2]. В то же время ранние белки ВПЧ активно синтезируются и инициируют процессы малигнизации инфицированных эпителиальных клеток. Поздние гены ВПЧ содержат кодоны, которые редко используются млекопитающими, из-за чего синтез капсидных белков вируса протекает медленно и в небольших количествах, тормозя развитие противовирусного иммунитета. Таким образом, в процессе эволюции сложился механизм, с помощью которого вирусная инфекция защищается от системного воздействия иммунитета хозяина.
Активация цитотоксических лимфоцитов выступает ведущим механизмом защиты в организме человека на внедрение ВПЧ-инфекции. Цитотоксическая иммунная реакция при CIN включает четыре этапа: фагоцитоз и презентацию антигенов ВПЧ цервикальными макрофагами, активацию хелперов Th1, активацию цитотоксических Т-лимфоцитов и уничтожение пораженных вирусом клеток. Доказательством актуальности клеточного иммунитета при ВПЧ служит факт сочетания спонтанного регресса, например бородавок с инфильтрацией окружающих их тканей лимфоцитами и макрофагами. Однако при супрессии клеточного звена иммунитета и уменьшении числа клеток Лангерганса происходит активация папилломавирусной инфекции. Длительной персистенции ВПЧ способствует установленная в ряде исследований способность вируса «ускользать» от системного иммунного надзора [6, 7]. Хотя ВПЧ, как уже было отмечено, инфицирует преимущественно базальные клетки, репликация вируса и сборка вирусных частиц происходят в дифференцированных клетках поверхностного слоя эпителиальных клеток. После репликации вирус выходит из клеток, подвергающихся последующему апоптозу, и указанный процесс не сопровождается признаками воспаления. Эффекторные клетки иммунной системы продуцируют ряд цитокинов, в т.ч. интерфероны-α, -β и -γ, которые снижают транскрипцию генов Е6 и Е7 у ВПЧ 16-го, 18-го и 33-го типов в трансформированных вирусами клетках [7].
В настоящее время не существует единой этиотропной терапии и практически отсутствует системное лечение пациентов с ВПЧ-ассоциированной инфекцией. Тем не менее сформулировано несколько принципов лечения данной группы заболеваний, следование которым позволяет достигать наилучших результатов.
Первым принципом лечения ВПЧ-ассоциированных заболеваний является комплексный подход, включающий использование различных методов деструкции гипер- и неопластических образований. Данные методы включают применение цитотоксических препаратов (подофиллин, подофиллотоксин и др.); химическую (трихлор-уксусная кислота, Солкодерм и др.) и физическую деструкцию (криодеструкция, лазеродеструкция, диатермокоагуляция, электрохирургический метод, фотодинамическая терапия).
Доказанное участие иммунных механизмов в развитии ВПЧ-инфекции, проявляющееся вторичным иммунодефицитом, служит обоснованием к использованию в ее терапии иммуномодулирующих лекарственных средств [7]. В связи с этим вторым принципом терапии ВПЧ-ассоциированных заболеваний является включение в план лечения иммунотропных средств разных групп и механизмов действия, позволяющих существенно повышать эффективность терапии, снижать частоту рецидивов и способствовать элиминации/эрадикации вируса. Необходимо отметить, что в числе иммуномодулирующих средств, применяемых для профилактики РШМ, в последние годы используют также и вакцину против ВПЧ.
Современная классификация иммуномодулирующих средств включает иммуномодуляторы микробного происхождения, природные и синтетические иммуномодуляторы, иммуномодуляторы на основе цитокинов. На сегодняшний день единственным иммуномодулирующим средством, рекомендованным европейским руководством по лечению дерматологических болезней, является инозин пранобекс, что указывает не только на особенности механизма его действия, но и на клиническую значимость этого лекарственного препарата [16].
Возможности применения препарата инозин пранобекс
Инозин пранобекс (Изопринозин), лекарственный препарат, сочетающий отчетливые иммуномодулирующие свойства с противовирусной активностью, был разработан .
По химическому строению инозин пранобекс является комплексным синтетическим препаратом, представляющим собой молекулярный комплекс, включающий инозин (гипоксантин-рибозид): пара-ацетиламинобензойная кислота (ацидобен): N,N-диметиламино-2-пропанол (димепранол)=1:3:3 комплекс.
Изопринозин относят к классу иммунофармакологических (иммунотропных) лекарственных препаратов, к группе иммуномодуляторов. Его основное действие – иммуномодулирующее, проявляется в восстановлении сниженной функции важнейших клеток иммунной системы – Т-лимфоцитов и моноцитов периферической крови. Следует отметить, что по физико-химическим свойствам препарат отличается от индивидуальных компонентов, образующих его структуру, что определяет различия в их фармакодинамике и фармакокинетике. Он более растворим, чем инозин, что улучшает его абсорбцию в желудочно-кишечном тракте и обладает заметно более высокой биологической активностью [8].
В клинических исследованиях препарат нормализует дефицит или дисфункцию клеточного иммунитета за счет повышения активности Th1-клеточного типа реакций, которые запускают созревание и дифференцировку Т-лимфоцитов, потенцируют лимфопролиферативные реакции в ответ на действие митогенов или клеток, активированных антигенами [7]. Кроме того, Изопринозин оказывает модулирующее влияние на цитотоксические эффекты Т-лимфоцитов и клеток – природных киллеров (NK-клеток), функции субпопуляций Т8-супрессоров и Т4-хелперов, повышает формирование на их плазматических мембранах поверхностных маркеров иммуноглобулина G и комплемента, нормализует соотношение между субпопуляциями Т-хелперов и Т-супрессоров, что рассматривается как восстановление иммунорегуляторного индекса CD4/CD8. Действие препарата сопровождается повышением продукции цитокинов иммунокомпетентными клетками, в частности, увеличивается образование интерлейкина-1 (ИЛ-1) и ИЛ-2, образование рецепторов к ИЛ-2. Его важными свойствами являются увеличение секреции эндогенного интерферона-γ, а также снижение биосинтеза ИЛ-4. Имеются данные о том, что Изопринозин потенцирует хемотаксис и фагоцитирующую активность нейтрофилов, моноцитов и макрофагальных клеток [9].
Молекулярные механизмы действия Изопринозина, в т.ч. определяющие противовирусные свойства, включают усиление подавленного/сниженного синтеза мРНК в лимфоцитах и осуществление в этих клетках процессов трансляции. Кроме того, Изопринозин в высоких концентрациях способен ингибировать активность цГМФ-фосфодиэстеразы. Указанные механизмы определяют противовирусную активность препарата, которая носит неспецифический характер и установлена в отношении значительного числа вирусов – простого герпеса I и II типов, герпеса Zoster, вируса Эпштейна–Барр, цитомегаловируса и др. [10].
Изопринозин относится к малотоксичным веществам и в этом отношении имеет преимущества перед другими синтетическими иммуномодулирующими средствами с противовирусной активностью. Фармакокинетика Изопринозина определяется строением и свойствами образующих его молекулу компонентов [11].
Препарат не обладает аллергизирующими, мутагенными, канцерогенными и эмбриотоксическими свойствами. Разрешен к применению детям и взрослым [12].
В медицинской практике Изопринозин начал применяться с 1973 г. в США, а с 1978 г. – в странах Европейского Союза. Под различными торговыми названиями препарат зарегистрирован в 73 странах в качестве лекарственного средства для лечения ряда вирусных и иммунодефицитных заболеваний, всего по 22 показаниям.
В Российской Федерации Изопринозин («Тева Фармацевтические предприятия Лтд.») был зарегистрирован в 1997 г.
Клинические исследования продемонстрировали хорошую переносимость Изопринозина. Побочные эффекты при его применении проявляются редко и представлены главным образом головными болями, тяжестью в области желудка, приливами жара. В отдельных случаях зарегистрировано небольшое повышение уровня мочевой кислоты в крови. Побочные эффекты устраняются при прекращении применения препарата [13].
Согласно инструкции по медицинскому применению Изопринозина, утвержденной Минздравсоцразвития РФ, показаниями к его применению в нашей стране является лечение гриппа и других ОРВИ; инфекции, вызванные вирусом герпеса 1-го, 2 и 3-го и 4-го типов: генитальный и лабиальный герпес, герпетический кератит, опоясывающий лишай, ветряная оспа, инфекционный мононуклеоз, вызванный вирусом Эпштейна–Барр; цитомегаловирусная инфекция; корь тяжелого течения; папилломавирусная инфекция: папилломы гортани/голосовых связок (фиброзного типа), папилломавирусная инфекция гениталий у мужчин и женщин, бородавки; контагиозный моллюск. Противопоказания к применению Изопринозина: повышенная чувствительность к компонентам препарата; подагра; мочекаменная болезнь; аритмии, хроническая почечная недостаточность; детский возраст до 3 лет (масса тела до 15–20 кг) [10, 19].
В ряде рандомизированных плацебо-контролируемых клинических исследований установлена высокая эффективность применения Изопринозина в лечении инфекций, вызываемых вирусом простого герпеса. Монотерапия в дозах 3–4 г/сут как короткими курсами (5–10 дней) до исчезновения симптомов заболевания, в бессимптомный период – по 1 таблетке 2 раза в день в течение 30 дней для уменьшения числа рецидивов [19]. Длительный прием на протяжении 6 месяцев в непрерывном режиме ведет к сокращению сроков острого периода, предупреждает повторные обострения в течение 12–24 месяцев [14]. При этом действие Изопринозина достоверно отличается от плацебо и по эффективности сопоставимо с действием противовирусного препарата ацикловир. Также выявлено, что препарат оказывает терапевтическое и профилактическое действия на ряд пациентов с герпетической инфекцией, устойчивой к терапии традиционными противовирусными препаратами [8].
Клинические исследования, посвященные моно- и комбинированной терапии Изопринозином кондилом наружных половых органов у мужчин и женщин (остроконечных, вульвовагинальных и эндоцервикальных кондилом, ассоциированных с ВПЧ), указывают на его 100%-ную эффективность, что связано с воздействием препарата на ВПЧ не только в труднодоступных для хирургического или лазерного воздействия участках локализации кондилом, но и в нервных ганглиях.
В острую фазу Изопринозин назначают по 50 мг/кг массы тела больного (6–8 таблеток в сутки, разделенных на 3–4 приема) в течение 14–28 дней, далее с трехкратным повторением указанного курса с интервалами в 1 месяц [11, 15, 19].
Изопринозин был изучен клинически и при обычных бородавках на руках и лице, плоских бородавках стопы. Установлено, что при использовании препарата в дозе 50 мг/кг/сут в течение от 7 до 60 дней (до очищения кожи от бородавок) его применение сопровождалось уменьшением либо отпадением бородавок указанных типов и очищением кожи. В рамках исследований было установлено также повышение в периферической крови числа Т-хелперов – CD4-лимфоцитов – и повышение соотношения клеток CD4/CD8-хелперов, подавляющих цитотоксические клетки иммунной системы [16].
Проведено клиническое изучение эффективности Изопринозина (50 мг/кг/сут) при папилломах гортани/голосовых связок (фиброзного типа) в комбинации с хирургическим удалением (лазерная хирургия) последних. Установлено, что прием препарата в течение 2 дней до операции и в течение последующих 8 дней сопровождается достоверным уменьшением частоты осложнений лазерной терапии, отсутствием кровотечения при выполнении операции, отсутствием или в незначительной степени выраженным отеком тканей гортани, устранением необходимости трахеотомии и улучшением голоса и речи пациентов после операции, а также снижением частоты рецидивов заболевания. Дополнительными результатами применения Изопринозина в комбинации с оперативным лечением являются упрощение и бóльшая эффективность оперативного удаления папиллом гортани [16]. Имеются данные, свидетельствующие об эффективном применении препарата детьми и взрослыми при лечении передающегося половым и бытовым путями инфекционного заболевания – контагиозного моллюска. Использование Изопринозина в дозе 50 мг/кг/сут в течение 10 дней как в монотерапии, так и в комбинации со стандартными методами наружной терапии приводит к разрешению кожных высыпаний как в острых, так и в хронических случаях заболевания. Эффективность терапии достигает более 75% [17].
Заключение
Таким образом, ВПЧ-ассоцииро-ванные заболевания гениталий являются широко распространенным видом патологии, имеющим большую медико-социальную значимость из-за высокого риска развития неопластических процессов, прежде всего РШМ. Экспериментальные и клинические исследования свидетельствуют о том, что иммунные механизмы играют важную роль в патогенезе ВПЧ-ассоциированных заболеваний и обусловленных ими вторичных иммунодефицитов, что позволило включить иммуномодулирующие лекарственные средства в арсенал терапевтических мероприятий при данных заболеваниях [18]. Результаты многочисленных клинических исследований свидетельствуют о том, что Изопринозин является препаратом, обладающим иммуномодулирующей активностью и неспецифическими противовирусными свойствами, показаниями к применению которого является ряд вирусных и иммунодефицитных заболеваний, в т.ч. ВПЧ-ассоциированных, и в гинекологической практике.
Можно ли применять ВИФЕРОН Свечи при ВПЧ вагинально?
Противовирусные суппозитории ВИФЕРОН выпускаются только для ректального использования. Вагинальное использование не предусмотрено в инструкции к лекарству. Применение в комплексной терапии препарата направлено на повышение уровня иммунной защиты организма в целом. Поэтому введение свечей непосредственно в очаг инфекции не требуется.
В прямой кишке присутствует множество кровеносных сосудов, всасывающих лекарство, непосредственно введенное в полость прямой кишки. Кровь от прямой кишки, минуя печень, непосредственно попадает в большой круг кровообращения. Таким образом обеспечивается системное действие препарата. Более того, печень не претерпевает дополнительной нагрузки, что является неоспоримым преимуществом препаратов с ректальным способом введения.
Лечение слизистой при ВПЧ у мужчин
При лечении проявлений вируса папилломы на слизистой у мужчин также применяются суппозитории ректальные ВИФЕРОН, которые помогут избавиться от неприятных проявлений вируса и будут способствовать укреплению иммунной системы.
Без консультации уролога не рекомендуется применять никакие лечебные кремы и мази, заниматься самолечением или вообще отказываться от терапии, назначенной врачом. При отсутствии лечения кондиломы могут разрастаться, охватывая все новые территории и поражая мочеиспускательный канал и другие внутренние органы. Предупредить развитие осложнений можно при помощи своевременного обращения к специалисту и применения противовирусных препаратов.
Какие продукты включить в рацион для укрепления иммунитета
Помимо стандартных фармацевтических препаратов, можно укреплять иммунную систему при помощи натуральных продуктов питания.
Разнообразьте свое меню продуктами, которые содержат:
- витамин A (фрукты и овощи красного, желтого и оранжевого цветов, яйца, печень, молочные продукты средней жирности);
- витамин B (орехи, семена, грибы, гречка, твердые сорта сыра);
- витамин C (цитрусовые, киви, шиповник, смородина, облепиха);
- витамин E (капуста, салаты, отруби, растительные масла холодного отжима, пророщенная пшеница).
Также не забывайте про такие микроэлементы, как цинк, йод, селен, кальций, железо: они в достаточном количестве содержатся в зелени, которой стоит дополнять практически каждый свой прием пищи, особенно обед и ужин (ужин может состоять именно из зелени – это легкий, хорошо усваиваемый и полезный прием пищи).
Вода – это еще один важный фактор, влияющий на эффективность лечения ВПЧ. Чем больше чистой воды будет поступать в ваш организм, тем интенсивнее он будет очищаться и избавляться от токсических веществ. Так силы организма будут направлены именно на защиту от инфекций, а не на борьбу с постоянно поступающими токсинами.
К природным и естественным продуктам-иммуномодуляторам, которыми стоит дополнить свой рацион, относятся:
- мед (для видимого эффекта – минимум 100 г в сутки, но не более 200 г, чтобы не перегружать поджелудочную железу);
- корень имбиря (лечебные чаи из него);
- чеснок (минимум 1 зубчик чеснока каждый день в течение 3-5 месяцев);
- прополис – вещество, производимое пчелами из сырья из древесных почек (профилактический курс длится около 45 дней);
- шиповник (содержит в 40 больше витамина C, чем лимоны);
- ромашковый, калиновый, клюквенный чай;
- соки из моркови, рябины;
- ягоды: малина, смородина, клубника, черника, кизил.
Альтернативные методы лечения ВПЧ на коже
Медикаментозная терапия проявлений вируса папилломы человека прекрасно сочетается с удалением новообразований в виде бородавок, папиллом на теле и кондилом, которые располагаются у мужчин и женщин в аногенитальной области (включая кожу гениталий, анус и слизистую оболочку влагалища, шейки матки, головки полового члена, прямой кишки).
Сегодня существует несколько продуктивных методов избавления от указанных новообразований, которые в большинстве своем безболезненны, безопасны и не оставляют шрамов.
Методы удаления папиллом и кондилом
Хирургическое иссечение
В настоящее время подобное вмешательство применяется нечасто, в основном используется при лечении злокачественных новообразований, когда необходимо широкое иссечение.
Медикаментозное удаление (прижигание) при ВПЧ
Это удаление наростов на коже при помощи лекарственных препаратов – растворов кислот, щелочей, солей. Новообразования на коже удаляются с помощью этих препаратов путем прижигания. Как правило, на месте удаления образуется корочка, которая отпадает в течение 5-7 дней. Полное заживление тканей происходит в течение 10-14 дней. При множественных новообразованиях могут потребоваться дополнительные процедуры.
Лазерное удаление папилломы
При этом способе удаления папилломы и кондиломы сжигаются при помощи луча лазера. При удалении не повреждаются соседние участки. После процедуры обычно остается микроскопичная ранка, которая заживает в течение 2-3 недель. Удалить лазером можно как единичные, так и множественных образования, расположенные на лице и теле, в том числе в деликатных местах (на веках, подмышками, в промежности).
Радиоволновое удаление при ВПЧ
При этом способе используют прибор Surgitron. Основная рабочая часть аппарата – электрод, который представляет собой тонкую вольфрамовую нить. На конце электрода концентрируются радиоволны высокой частоты. Воздействуя на органическую ткань, пучок волн приводит в движение молекулы воды в клетке, вследствие чего происходит разрыв клетки и она испаряется, в результате происходит «холодный» разрез тканей на нужном участке кожи или слизистой. При этом окружающие ткани, сосуды остаются неповрежденными, что в некоторых случаях позволяет избежать обильного кровотечения. После разреза радионожом на операционной ране образуется фибриновая пленка, а затем корочка, которая постепенно сходит и остается незаметный рубец.
Криодеструкция папиллом
Криодеструкция папиллом заключается в точечном воздействии на образование очень низкой температурой (около -196° С). Для этого обычно применяется жидкий азот и специальная металлическая точечная насадка, выполняющая роль проводника. Во время такой процедуры клетки папилломы погибают. Здоровые ткани в области ее формирования покрываются небольшой коркой, которая через небольшой промежуток времени отваливается.
Электрокоагуляция папиллом при ВПЧ
Этот метод предусматривает удаление патологических тканей путем воздействия на них электрическим током. Процедуру проводят при помощи специальных аппаратов, оснащенных электродом или петлей, которые нагреваются под воздействием электрического тока до высоких температур. На месте удаленной бородавки также образуется корочка, которая со временем отпадает.
Все методы удаления папиллом и кондилом имеют свои плюсы и минусы, оценить которые можно только со своим лечащим врачом с учетом индивидуальных особенностей пациента. Применение любых рецептов народной медицины, найденных на просторах интернета, также допускается только после консультации со специалистом.
Таблеток и процедур, которые раз и навсегда избавят от вируса папилломы человека, пока не существует. Однако уже сегодня существуют препараты и методы лечения, которые помогут сократить рецидивы проявлений инфекции или вообще забыть о них.
Справочно-информационный материал
Автор статьи
Беляев Дмитрий Александрович
Врач общей практики
Loading …
Пройти другие опросы
VISION: эффективность + натуральность
Объединить высокую эффективность со 100 %-ной натуральностью состава, удалось компании Vision. Она создала ряд БАДов с иммуномодулирующими свойствами: они активно стимулирую иммунную систему, укрепляют и очищают организм, не причиняя при этом никакого вреда и не вызывают побочных эффектов.
В чем особенность продукции Визион:
- в полностью натуральном составе, в который входит растительное сырье, выращиваемое на экологически чистых территориях нашей планеты;
- в уникальной технологии сушки и криогенного дробления растительного сырья, благодаря которой по максимуму сохраняются все ценные вещества, витамины и минералы;
- в высокой степени усвоения (около 98 %);
- в отсутствии противопоказаний и побочных явлений;
- в мягкой и корректной стимуляции иммунитета, за счет чего после терапии иммунная система продолжает работать самостоятельно;
- в высоком качестве продукции, которое соответствует стандартам GMP и ISO22000.
Все препараты Вижен сертифицированы Минздравом и исследованы в ходе клинических испытаний, проводимых на базе института РФ: НИИИ питания РАМН.
Ознакомиться со всеми сертификатами, результатами исследований и прочей документацией, подтверждающей качество и безопасность биодобавок, можно на официальном сайте компании.
Лечение папиллом (6, 11 и многих других штаммов, которых всего насчитывается 180) иммуномодуляторами Vision происходит легко, без нарушения функционирования организма и грубого воздействия на работу основных систем, как это происходит при лечении синтетическими препаратами.
Помните, что даже самый качественный иммуномодулятор при папилломах — это не панацея, а лишь хорошее дополнение к основному лечению, если оно требуется. Их нужно употреблять только в комплексе.