Быстрый переход Лечение атопического дерматита у детей
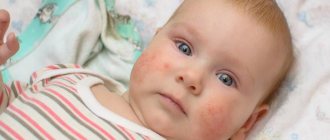
Атопический дерматит — это заболевание, при котором кожа сильно зудит, становится раздраженной, красной, сухой, имеет неровности.
Атопический дерматит — распространенное кожное заболевание, входящее в группу болезней кожи, объединенных более широким термином «экзема».
Существуют и другие типы экземы: нумулярная, дисгидротическая и т. д. Тем не менее, термины «экзема» и «атопический дерматит» часто используют как синонимы.
Как правило, атопический дерматит дебютирует в младенческом возрасте (в 3–6 месяцев) и встречается у 15–20 % детей. Чаще всего его течение максимально тяжелое в первые 1–3 года жизни, по мере взросления ребенка тяжесть болезни снижается. Обычно атопический дерматит исчезает к школьному возрасту или периоду полового созревания. Однако у некоторых людей заболевание может сохраняться всю жизнь, изредка обостряясь, или проявляясь постоянно.
Каковы причины болезни?
Следует различать причину и триггеры атопического дерматита.
Причина до конца не известна современной науке, основной версией является набор генетических, иммунных и кожных изменений, в частности, дефицит кожного белка филаггрина, который отвечает за удержание влаги в коже.
Триггеры атопического дерматита весьма разнообразны, атопическая кожа чрезмерно чувствительна к раздражению, поэтому обострение могут вызвать повышенное потоотделение, жара, грубая одежда, моющие средства, сухость воздуха и т. д. Дети с атопическим дерматитом могут параллельно иметь аллергию на продукты питания, домашних или других животных, пылевых клещей, пыльцу деревьев и травы — эти аллергены также могут являться триггерами обострений.
В целом атопический дерматит имеет волнообразное течение, периоды обострений (чаще всего возникающие по неочевидным причинам или без причин) сменяются периодами ремиссии — отсюда появляется большой соблазн связывать обострения с факторами, не имеющими прямого отношения к болезни, и наоборот — приписывать лечебные свойства совершенно посторонним факторам (например, диете, которую родители начали по ошибке или от отчаяния).
Нельзя не упомянуть устоявшуюся вредную отечественную традицию называть атопический дерматит аллергическим (обычно связывая его с аллергией на белок коровьего молока) и лечить его диетами (строгая «гипоаллергенная» диета кормящей матери, и/или гидролизная/аминокислотная смесь ребенку). Действительно, если у ребенка есть непереносимость белков коровьего молока, она может усугублять или вызывать атопический дерматит, но не наоборот. Далеко не каждый ребенок с атопическим дерматитом имеет непереносимость белков коровьего молока или каких-либо других аллергенов. А значит, назначая диету, или дорогую и неприятную на вкус смесь, врач добавляет семье проблем, не помогая им. В большинстве случаев атопического дерматита выявление аллергий и исключение аллергенов не приносит никакой пользы.
Причины появления аллергического дерматита
Аллергический дерматит включает в себя множество воспалительных процессов на кожных покровах, связанных с негативным воздействием раздражителей, чаще – пищевых аллергенов. Очень часто заболевание провоцируется некоторыми продуктами питания – патоген проникает в кровеносную систему через желудочно-кишечный тракт. Также стоит отметить косвенные причины, которые также могут вызывать симптомы аллергического дерматита. К ним относятся:
- генетическая предрасположенность;
- гормональные нарушения;
- дефицит в организме витаминов и минералов;
- несбалансированное питание;
- стресс и нервное перенапряжение;
- психические расстройства;
- физические перегрузки;
- аутоиммунные заболевания;
- сбои в функциях желудка.
Также на развитие заболевания влияет окружающая среда – в регионах с плохой экологией пациентов с данной патологией больше, чем в районах с благоприятной экологической ситуацией.
Проявления атопического дерматита
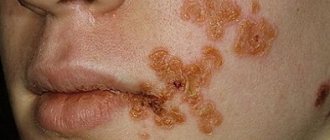
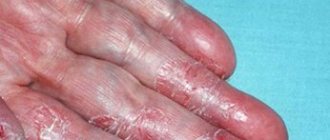
Кожные симптомы и локализация поражений различаются у детей разного возраста. Общие симптомы — появление на коже красных, сухих, зудящих пятен, которые возникают в результате воспаления. Обязательно присутствует зуд — от легкого до невыносимого, нарушающего сон и аппетит. При частом расчесывании на коже могут образовываться царапины (расчесы), мокнутия (отделение серозного экссудата через мельчайшие дефекты эпидермиса), корки или эрозии из-за вторичной инфекции. Иногда, если атопические поражения кожи, поражения от хронического зуда и вторичной инфекции длятся многие недели, могут развиваться очаги атрофии кожи (шрамы, гипопигментация/гиперпигментация, истончение или утолщение кожи).
У младенцев атопический дерматит обычно поражает лицо, кожу волосистой части головы, руки и ноги. У детей старшего возраста, как правило, поражаются только локтевые сгибы, подколенные ямки и запястья. У некоторых детей с тяжелой формой болезни может поражаться все тело. Экзема вызывает сильный зуд, способный в свою очередь приводить к ряду вторичных проблем: нарушениям сна, потере веса, депрессии (у ребенка или у взрослого, который за ним ухаживает) и т. д.
Симптомы обычно ухудшаются в осенне-зимний период (этот факт принято связывать с включением центрального отопления и более суровыми внешними климатическими условиями) и улучшаются в весенне-летний период, а также на морских курортах (это принято связывать с обилием ультрафиолета и более мягкими климатическими влияниями на пораженную кожу). Обычно наиболее тяжелое течение болезни отмечается у детей в возрасте 6–18 месяцев (зимой обострения чаще и тяжелее, летом — реже и легче), затем год от года обострения все реже, протекают легче. К школе большинство детей выздоравливают или имеют проявления, не снижающие качество жизни.
Современный взгляд на базовый уход за кожей детей при атопическом дерматите
Введение
Атопический дерматит (АтД) – это хроническое воспалительное заболевание кожи. АтД, как наиболее распространенный из дерматитов, поражает до 20% детей и 1–3% взрослых в большинстве стран мира [2]. В 50% случаев первые симптомы АтД появляются в первые 6 мес. жизни, и в 90% − до 1 года [3]. Точные механизмы патогенеза АтД до настоящего времени остаются невыясненными. Принято считать, что возникновение АтД связано с генетически обусловленным нарушением защитного барьера кожи, нарушением работы иммунной системы, инфекцией и условиями окружающей среды. По данным многих исследований ведущим механизмом в патогенезе развития АтД является дисфункция эпидермального барьера [4]. Целью базового ухода (терапии) при АтД является восстановление и поддержание нормальной структуры и функции эпидермального барьера, что позволяет предотвратить сенсибилизацию, инфицирование и продлить ремиссию. Последние научные данные о нарушении защитных функций кожи позволяют лучше понять течение болезни и подобрать адекватную терапию, включающую обязательный базовый уход за кожей. АтД – в первую очередь проблема педиатров, т. к. в основном пациентами являются дети раннего возраста. Педиатры ведут примерно 30% пациентов с АтД [5], поэтому они нуждаются в информации об особенностях таких детей и, в первую очередь, о современных средствах базового ухода за кожей своих маленьких пациентов.
Целью
данной работы является обозначение роли и значимости простого алгоритма базового ухода за кожей детей при АтД, а также рассмотрение вопросов применения специализированных косметических средств в зависимости от индивидуального статуса кожи пациента и условий окружающей среды.
Эпидермальный барьер: структура и функции
Эпидермальный барьер – собирательное понятие, которое характеризует состояние рогового слоя и протекающие в нем процессы [4]. Осуществление барьерных функций кожи обеспечивается посредством взаимодействий различных функциональных структур. В таблице 1 приведены основные структурные элементы эпидермального барьера и их функции.
Верхний слой кожи, роговой слой (Stratum Corneum), является основным компонентом эпидермального барьера (рис. 1). Именно роговой слой служит барьером на пути проникновения в глубокие слои кожи раздражающих веществ и аллергенов. Роговой слой состоит из плоских клеток без органелл и ядра – корнеоцитов, являющихся конечной стадией дифференцировки клеток эпидермиса (кератиноцитов). Его структурная целостность поддерживается благодаря наличию корнеодесмосом, которые обеспечивают связь корнеоцитов между собой. Согласно представлениям роговой слой – это структура «кирпич − цемент», в которой роль строительных блоков выполняют корнеоциты, а строительного раствора – липиды межклеточного матрикса. В расширении модели корнеодесмосомы выполняют роль «железных прутьев», которые придают структуре надлежащую жесткость [4]. Ближе к поверхности кожи корнеодесомосомы исчезают, роговой слой становится более рыхлым, и корнеоциты слущиваются.
Рис. 1. Нормальное состояние эпидермального барьера
Процесс формирования эпидермального барьера начинается на границе между зернистым слоем и роговым слоем: из кератиносом (ламеллярных телец) секретируются липидные предшественники вместе с ферментами [7]. Липидный матрикс
имеет решающее значение в выполнении роговым слоем своей защитной функции. Основное назначение этого матрикса – предотвратить чрезмерное испарение воды через эпидермис и развитие ксероза. С одной стороны, он обеспечивает целостность и эластичность кожи, а с другой – препятствует проникновению водорастворимых веществ в глубокие слои эпидермиса. В состав липидного матрикса входят 3 вида соединений: церамиды (сфинголипиды), холестерин и жирные кислоты в приблизительно равных молярных количествах. Церамиды представляют собой полярные липиды, именно благодаря этому они способны образовывать упорядоченные, плотно упакованные бислои − ламеллы [8, 9]. Установлено, что в липидном матриксе присутствуют как трехмерные структурированные участки (называемые кристаллической фазой), так и неструктурированные (жидкокристаллическая фаза), причем для выполнения барьерной функции кожи одинаково важны состав этих ламеллярных слоев и их взаимное расположение [8−10]. Этот матрикс устойчив к факторам обезвоживания, к изменению температуры и давлению благодаря гетерогенному составу полярных липидов и высокой концентрации холестерина, стабилизирующего жидкокристаллическую фазу [11]. По мере упорядочения структуры рогового слоя от нижней границы к поверхности кожи уменьшается и содержание воды, в верхних слоях рогового слоя ее остается всего лишь 10%. Роговой слой – это единственная структура в организме, где межклеточное пространство заполнено в основном липидами, а не водой! Химические соединения, входящие в состав межклеточного матрикса и обеспечивающие его гидратацию, образуются путем сложных биохимических процессов из особого белка − филаггрина, который, в свою очередь, формируется из профилаггрина в зернистом слое эпидермиса [12]. Следует отметить, что функции этого белка неодинаковы в нижних и верхних уровнях рогового слоя. Ближе к границе с зернистым слоем он способствует механической прочности барьера путем вовлечения в формирование корнеоцитов. А в верхних участках рогового слоя филаггрин распадается на свободные аминокислоты, мочевину, пироглутамат натрия, которые известны под названием Натуральный Увлажняющий Фактор (Natural Moisturizing Factor, NMF). Эти соединения находятся в непосредственной близости от корнеоцитов и играют важнейшую роль в обеспечении нормального уровня гидратации кожи. Также они формируют кислую среду, необходимую для баланса между скоростью созревания кератиноцитов и скоростью десквамации корнеоцитов, а также для уменьшения вероятности колонизации поверхности кожи патогенными микроорганизмами [12]. Необходимо отметить, что синтез филаггрина и его распад – это очень тонкий баланс между его производством и протеолизом, с одной стороны, и ингибированием этих процессов – с другой. От этого баланса во многом зависит целостность и функционирование эпидермального барьера. Известно, что уровень кислотности кожи является ключевым фактором в формировании эпидермального барьера, целостности рогового слоя и антимикробной защиты. Во-первых, в формировании эпидермального барьера участвуют рН-зависимые ферменты. Активность сериновых протеаз является значимой частью нормального функционирования кожи: с одной стороны, эти ферменты участвуют в преобразовании предшественников липидов в их активную форму, с другой – способствуют разрушению корнеодесмосом и регулированию процесса десквамации [13]. Во-вторых, ламеллярные слои образуют кристаллическую структуру только при рН 4,5−6,0 [14]. В-третьих, синтез антимикробных пептидов в кератиноцитах и клетках потовых и сальных желез также является рН-зависимым процессом, равно как и размножение бактерий на поверхности эпидермиса [13, 15, 16].
Кожа детей
раннего возраста отличается от кожи взрослых; процесс ее созревания продолжается, как минимум, в первый год жизни ребенка. Это касается структурных отличий в строении (более мелкие клетки, более тонкие слои) эпидермиса и дермы, концентрации NMF, уровнях гидратации и рН [17, 18]. У детей до 2-х лет в среднем эпидермис на 20% тоньше, чем у взрослых, а роговой слой – на 30% [19]. Меняется состав как NMF, так и липидного матрикса. При рождении кожа ребенка более сухая, чем у взрослых, однако в возрасте 3−24 мес. уровень ее гидратации значительно превышает таковой у взрослых. Кожа быстро абсорбирует воду, но так же быстро ее и теряет. Формирование кислой среды в роговом слое, как было указано выше, является основой для нормального функционирования эпидермального барьера. В норме рН поверхности кожи составляет 4−6, более глубокие слои эпидермиса примерно рН-нейтральные [13]. У новорожденных рН поверхности кожи 6,5−7,5, однако в течение первых 2-х недель жизни рН снижается и становится примерно равным таковому у взрослых людей. Следует также отметить, что микробный пейзаж кожи претерпевает радикальные изменения в течение 1-го года жизни [17]. Младенческая кожа демонстрирует повышенную проницаемость для раздражителей и более восприимчива к инфекциям. Таким образом, кожа детей отличается от кожи взрослых, и процесс созревания эпидермального барьера занимает от нескольких месяцев до нескольких лет после рождения.
Нарушение эпидермального барьера при АтД
Изменение барьерных функций кожи при АтД связано с увеличением проницаемости эпидермального барьера и характеризуется изменением структуры и состава липидного матрикса рогового слоя, а также снижением концентрации компонентов NMF [4, 8–10]. Степень нарушения целостности барьера определяют повышение трансэпидермальной потери воды (transepidermal water loss, TEWL) и заметное снижение уровня гидратации кожи (рис. 2).
Рис. 2. Нарушение эпидермального барьера за счет потери влаги при АтД
В таблице 2 приведены основные нарушения барьерных функций кожи при АтД.
По мнению многих авторов, ведущую роль в нарушении барьера играет генетический дефект синтеза филаггрина, однако он не является единственным патогенетическим фактором [3, 4, 9]. По мере снижения синтеза филаггрина как предшественника компонентов NMF уменьшается увлажненность кожи, меняется рН и, как следствие, уменьшается активность протеолитических ферментов [13, 14]. Изменение рН на поверхности рогового слоя приводит к изменению микробного пейзажа и частому инфицированию [15]. Заметные изменения в составе липидов рогового слоя вызывают увеличение проницаемости барьера и TEWL [6, 20]. Отмечено, что низкие уровни церамидов и дисбаланс в их соотношении наблюдаются не только на участках пораженной кожи: даже в неповрежденной на вид коже при АтД происходят неблагоприятные изменения, уровень ее гидратации снижен, выражен ксероз [21, 22]. Свой вклад в ухудшение барьерных функций кожи вносит неконтролируемое и нерациональное применение наружных топических глюкокортикостероидов: их длительное использование вызывает атрофию кожи [4, 23, 24]. Зуд при АтД
Сухость кожи при АтД способствует проникновению патогенных микроорганизмов, аллергенов и раздражающих веществ, что приводит к развитию воспаления, сопровождающегося зудом, расчесыванием и дальнейшим повреждением кожи, запуская цикл «зуд − расчесывание» [25, 26]. Зуд − одна из основных проблем, значительно ухудшающих качество жизни при АтД и больных детей, и их родителей. От 30 до 90% детей с АтД испытывают зуд, который обостряется ночью [26], соответственно нарушается сон ребенка: до 84% детей страдают от ночных пробуждений [27].
Коррекция эпидермального барьера: роль специализированных косметических средств
Проведенные за последние десятилетия исследования роли эпидермального барьера в патогенезе АтД заставили обратиться к разработке методов его восстановления и поддержания нормального уровня. Термин «коррекция эпидермального барьера» приобрел большую значимость среди врачей и пациентов. Под ним подразумевают, во-первых, уменьшение сухости кожи − основного признака нарушения барьера и, во-вторых, воздействие на более глубокие слои эпидермиса с целью нормализации состояния липидного матрикса [28]. Более того, в комплекс ухода включаются очищение кожи и мероприятия по предупреждению запуска цикла «зуд − расчесывание» [29, 30]. В методических рекомендациях по ведению пациентов с АтД базовый уход (базовая терапия) с применением увлажняющих и смягчающих средств давно занимает ведущее место [1, 2, 29, 31–36]. Более того, в ряде рекомендаций обосновывается необходимость использования специализированных увлажняющих и смягчающих средств – эмолентов у детей с высоким риском развития АтД непосредственно с рождения [37, 38]. Наиболее эффективным способом восстановления защитной функции эпидермиса служит применение косметических средств, восстанавливающих структуру рогового слоя эпидермиса и предотвращающих избыточную TEWL [39]. Необходимо отметить, что для ухода за атопичной кожей не подходят обычные косметические средства. Для коррекции состояния кожи разрабатываются специализированные косметические средства. Общее правило рецептур специализированной косметики заключается в использовании гипоаллергенных активных ингредиентов с подтвержденной эффективностью и безопасных консервантов, исключении потенциально сенсибилизирующих компонентов (отдушек, красителей). Основа для такой косметики должна быть произведена из тщательно очищенного сырья и быть высокой, так называемой фармакопейной степени чистоты.
Алгоритм базового ухода за кожей при АтД
Основной принцип ухода за пораженной кожей заключается в постоянном использовании средств ухода − и в периоды обострения заболевания, и во время ремиссии. Существуют общие правила ухода и их вариации в зависимости от фазы болезни [35]. Основные правила базового ухода за кожей просты и понятны (рис. 3): 1) бережное очищение; 2) увлажнение и смягчение; 3) предупреждение раздражения и зуда.
Купание
рекомендуется для пациентов с АтД как часть ухода за кожей (сила рекомендаций С, уровень достоверности III) [31]. Купание ребенка с АтД не только очищает кожу от загрязнений, потенциальных аллергенов и патогенных микроорганизмов, но и увлажняет ее. Очищение кожи во время купания должно производиться тщательно, но осторожно. Результаты клинических исследований и методические рекомендации по частоте купания противоречивы [40], но в основном ведущие специалисты склоняются к необходимости ежедневного купания длительностью около 5 мин при температуре воды 27−30°С [2, 33]. Следует понимать, что неправильное использование средств для купания может привести к усилению сухости кожи и прогрессированию нарушения эпидермального барьера. Твердое, кусковое мыло имеет щелочную реакцию, и его использование при АтД не показано. Рекомендуется применение жидкого мыла, гелей для купания на основе мягких поверхностно-активных веществ, с рН 5,5−6,0 [1, 33, 40]. В течение 3 мин после купания на кожу следует нанести эмоленты – увлажняющие и смягчающие косметические средства (сила рекомендаций B, уровень достоверности II) [31] – «правило 3-х минут».
Применение топических увлажняющих средств и эмолентов
является важнейшим условием предотвращения и купирования сухости кожи (ксероза) при АтД (сила рекомендации А, уровень доказательности I) [31, 33]. Более того, установлено, что использование эмолентов может снизить потребность в местном применении глюкокортикостероидов и облегчить зуд [41]. В обзоре индексированных в базе данных клинических исследований (MEDLINE, Embase), посвященных использованию эмолентов в терапии АтД, (Lindh et al., 2015) приведены данные 595 публикаций (48 клинических исследований, 3262 пациента с АтД и ихтиозом). Подавляющее количество исследований подтвердило, что эмоленты благотворно влияют на клинические симптомы АтД и рекомендованы в качестве 1-й линии ведения пациентов с АтД [42]. В таблице 3 приведены основные типы косметических средств, используемых для увлажнения и смягчения кожи.
В зависимости от индивидуального статуса кожи, сезонных и климатических условий рекомендуется подбирать соответствующий уход. Зимой и при наличии сильного ксероза более оправданно применение безводных средств или окклюзивных формул «вода-в-масле», а для ухода за сухой кожей в летний период рекомендуются легкие кремы-эмульсии «масло-в-воде» с высоким содержанием влагоудерживающих компонентов [1, 32, 42]. Окклюзивные ингредиенты вазелин и минеральное масло широко применяются в формулах кремов при АтД благодаря их химической инертности, безопасности и высокой способности снижать TEWL [43, 44]. Особенно важно высокое содержание этих компонентов в рецептурах зимней защитной косметики [2]. Так называемые «кремы-без-масла» (oil-free) разрабатываются на основе силиконов. Увлажняющие косметические ингредиенты – это соединения с одной или несколькими гидроксильными группами, способные связывать и удерживать молекулы воды. Они могут привлекать воду как из нижних слоев эпидермиса, так и из окружающей среды, если влажность воздуха превышает 70% [6]. В средствах, рекомендованных при АтД, увлажнители самостоятельно не используются, т. к. могут увеличить TEWL, поэтому их сочетают в формулах с окклюзивными компонентами. Один из самых широко применяемых ингредиентов – мочевина. Она является физиологическим веществом, родственным нашей коже. Кремы с мочевиной используются в зависимости от ее концентрации (от 5 до 10%), типа кожи и уровня ее сухости. Применение средств, содержащих мочевину, в некоторых рекомендациях ограничено по возрасту и показано только с 3-х лет [32, 33]. Часто применяемый в кремах-эмолентах пропиленгликоль не рекомендуется в формулах для детей до 2-х лет [2]. Эмоленты – особый класс косметических ингредиентов, структура которых близка или подобна структуре липидов рогового слоя и себума. (По их названию часто называют и косметические средства, их содержащие.) Это гидрофобные соединения, способные заполнять дефекты липидного матрикса рогового слоя. Наиболее широко известны работы Р. Elis, который предложил использовать смеси физиологических липидов (церамиды, холестерин и смесь жирных кислот) для липидозаместительной терапии [10]. Помимо увлажняющих и смягчающих активных компонентов часто в специализированные кремы добавляют противовоспалительные и противозудные ингредиенты
. Бисаболол, гель алоэ-вера, масло Ши, кокосовое масло, экстракт виноградных косточек, глицирризиновая кислота, ниацинамид (витамин В3), пальмитилэтаноламид, соли магния и цинка обладают подтвержденными противовоспалительными свойствами и входят в рецептуры многих известных специализированных средств для базового ухода за кожей при АтД [22, 44, 46]. Следует отметить, что во всех рекомендациях указывается на необходимость частого и большого расхода эмолентов – 150−200 г в неделю для детей [1, 2, 31, 32]. Но действительность такова, что многие родители либо не используют эмоленты вообще, либо используют в недостаточном количестве. Так, в программе по обучению родителей, имеющих детей с АтД (Cork et al., 2003), отмечено, что 24% детей с АтД не получали базовый уход, а средний расход в группе пробандов был всего лишь 54 г в неделю. После обучения родителей и получения ими правильных рекомендаций было отмечено снижение симптомов тяжести АтД на 89% [47]. В Великобритании 12-недельная обучающая программа показала, что при увеличении расхода эмолентов наблюдается значительное снижение выраженности симптомов АтД и нормализация сна у детей без увеличения семейных расходов [48]. Важно отметить, что наиболее частой ошибкой педиатров при лечении пациентов с АтД, а также родителей при уходе за этими детьми является недостаточное внимание к уходу за кожей в период ремиссии. Врачу при рекомендациях по профилактике обострений необходимо делать акцент на обязательном непрерывном использовании увлажняющих и смягчающих средств, несмотря на стихание обострения или ремиссию заболевания.
Заключение
Ухудшение барьерных функций кожи при АтД связано с увеличением проницаемости эпидермального барьера и характеризуется изменением структуры и состава липидного матрикса рогового слоя, а также уменьшением концентрации компонентов NMF, о чем свидетельствует заметное снижение гидратации кожи и увеличение TEWL. В настоящее время целесообразность и необходимость использования специализированных косметических средств для восстановления барьерной функции кожи при легкой и средней степени тяжести АтД не вызывает сомнений. Современный алгоритм базового ухода за кожей включает бережное очищение, увлажнение и смягчение, а также предотвращение зуда как при обострении, так и в период ремиссии. Правильное и грамотное применение педиатрами и родителями пациентов этой простой и понятной схемы является важным фактором продления ремиссии, улучшения состояния кожи и самочувствия малыша.
Диагностика
Специального анализа или обследования для подтверждения диагноза атопический дерматит не существует, диагноз ставится клинически. Врач осмотрит сыпь, спросит о симптомах ребенка, семейном атопическом и аллергическом анамнезе. Наличие экземы у членов семьи (в детском возрасте или до сих пор) будет важным ключом к разгадке.
Врач исключит другие состояния, которые могут вызвать воспаление и зуд кожи. В случае затруднений с диагнозом или тяжелого течения болезни педиатр направит ребенка к детскому дерматологу или детскому аллергологу.
Врач может попросить исключить из рациона ребенка некоторые продукты (например, яйца, молоко, сою или орехи) на 2–3 недели, после чего снова ввести их в рацион и наблюдать за симптомами. Если диета приводит к облегчению сыпи, а провокация к ее явному обострению, это подтвердит диагноз и необходимость диеты.
Поскольку точных лабораторных методов подтверждения диагноза атопического дерматита нет, существуют критерии для стандартизации постановки клинического диагноза (самые известные — критерии Ханифина и Райки).
Критерии делятся на «большие» и «малые». Для постановки диагноза атопический дерматит необходимым и достаточным является обнаружение у пациента трех больших и трех малых критериев.
К большим относятся:
- зуд;
- дерматит, поражающий сгибательные поверхности у взрослых, или лицо и разгибательные поверхности у младенцев;
- хроническое или рецидивирующее течение дерматита;
- наличие в личном или семейном анамнезе кожной или респираторной аллергии.
К малым относятся:
- специфические черты лица: бледность лица, эритема, гипопигментированные пятна, темные круги под глазами, хейлит, подглазничные складки, рецидивирующий конъюнктивит, передние складки шеи;
- типичные триггеры: эмоциональные факторы, факторы окружающей среды, еда, раздражители кожи;
- типичные осложнения: восприимчивость к кожным инфекциям, нарушение клеточного иммунитета, предрасположенность к кератоконусу и передней субкапсулярной катаракте, немедленная реактивность кожи;
- другие признаки: ранний возраст дебюта, сухость кожи, ихтиоз, гиперлинейность ладоней, пилиарный кератоз, дерматит кистей и стоп, экзема сосков, белый дермографизм, белый питириаз, перифолликулярная акцентуация.
Пояснение каждого из этих симптомов выходит за рамки этой статьи; критерии приведены здесь для понимания того, чем руководствуется врач, выставляя диагноз атопического дерматита.
Также существуют различные шкалы оценки тяжести атопического дерматита, применяемые врачами и учеными, самой известной из них является шкала SCORAD. В этой шкале врачу необходимо отметить количество, распространенность и выраженность симптомов атопического дерматита, выразить их в баллах, суммировать баллы и на основе этой суммы выставить степень тяжести болезни.
Препараты «Акридерм ГК» при аллергическом дерматите
Комбинированный состав наделяет препарат «Акридерм ГК» широкими возможностями применения.[4] В него входят топические глюкокортикостероиды , которые показывают свою высокую степень эффективности в борьбе с проявлениями атопической и аллергической патологий. Данные средства – это мощный удар по воспалительному очагу, так как в составе препаратов «Акридерм ГК» сразу три действующих вещества:
- Бетаметазон – оказывает противовоспалительное, противоаллергическое, антиэкссудативное и противозудное действие.
- Гентамицин – оказывает бактерицидное действие.
- Клоримазол – имеет выраженное противогрибковое действие.
Следовательно, мазь и крем «Акридерм ГК» оказывает всестороннее воздействие на пораженные болезнью участки кожи, способствуя ее восстановлению и улучшению состояния больного. Препараты снимают зуд, покраснение и воспаление и помогает устранять патогенные микроорганизмы. Эти препараты можно использовать для лечения как острой фазы, так и хронического воспаления. И мазь, и крем хорошо впитываются в кожу, глубоко проникают в очаг. Для более точного выбора подходящего препарата рекомендовано обратиться к специалисту.
Лечение атопического дерматита у детей
Не существует полноценного лечения атопического дерматита, то есть нет таких методов терапии, которые привели бы к полному выздоровлению (изменили долгосрочный прогноз болезни). Все существующие методы терапии изменяют лишь краткосрочный прогноз — на ближайшие месяцы.
Тем не менее, лечение необходимо:
- для улучшения качества жизни ребенка и семьи; для профилактики вторичных местных осложнений (инфекций, атрофии кожи и др.);
- для профилактики психологических проблем (нарушений сна, депрессии и др.).
Лечение делится на изменение быта (устранение триггеров) и лекарственные вмешательства (устранение симптомов).
Изменение быта. Что родители могут сделать сами?
Не позволяйте коже вашего ребенка становиться чрезмерно сухой, не допускайте тяжелого зуда, избегайте факторов, вызывающих обострения. Попробуйте следовать этим простым советам:
- Детям с атопическим дерматитом следует принимать ванну короткое время или предпочитать душ с теплой (не горячей) водой. Используйте мягкое мыло без запаха или очищающие средства без содержания мыла. Не вытирайте, а промакивайте кожу полотенцем после мытья. Сразу после купания наносите увлажняющий крем на всю кожу. Подросткам предпочтительно пользоваться косметикой без запаха и увлажняющими средствами для лица без масла.
- Посоветуйтесь со своим врачом, если у ребенка нет противопоказаний, добавляйте в ванну при купании отвар овса, он способен снижать зуд.
- Следует отдавать предпочтение мягкой детской одежде из «дышащих» тканей, например хлопка. Шерсть или полиэстер могут быть слишком жесткими или раздражающими для атопической кожи.
- Ногти ребенка следует регулярно и коротко подстригать, чтобы предотвратить расцарапывание кожи. Если ребенок царапает себя ночью, постарайтесь укладывать его на сон в удобных легких варежках или с зашитыми рукавами пижамы.
- Следует избегать перегрева детей, так как пот может приводить к обострениям. Это особенно актуально для российских родителей, привыкших к жаркой температуре в квартире и перекутыванию детей на прогулках.
- Детям следует предлагать пить много воды.
- Постарайтесь избавиться от частых аллергенов в вашем доме и вне его, таких как пыльца, плесень и табачный дым.
- Стресс может усугублять атопический дерматит. Помогите своему ребенку найти способы справляться со стрессом (например, физические упражнения, глубокое дыхание или разговоры с психологом).