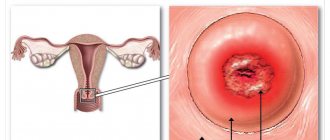
Вирус папилломы человека, общепринятая аббревиатура – ВПЧ.
Это возбудитель наиболее распространенной во всем мире инфекционной патологии слизистых и кожных покровов, т.н. папилломавирусной инфекции.
Существует порядка 200 типов данного вируса.
Примерно пятая часть из которых может передаваться при сексуальных контактах, повреждая органы урогенитальной системы.
Особую настороженность данный возбудитель вызывает из-за связи заражения и онкологических патологий.
Так, 93% эпизодов рака маточной шейки у женщин обусловлены именно этим вирусом, из которых 70% – ВПЧ 16, а также 18-го типов.
Вот почему, если у женщины при проведении обследования ВПЧ 16 обнаружено в анализах, врач настоятельно рекомендует дополнительные исследования.
Так что это такое: ВПЧ 16 генотип у женщин?
Все папилломавирусы условно разделяют на три основные группы в зависимости от их онкогенной опасности:
- неонкогенные, провоцирующие бородавки плоские/подошвенные/вульгарные (типы 1, 3, 2, 4, 41, 10 и др.), не способны вызывать злокачественные преобразования
- риска низкого, обуславливающие развитие аногенитальных бородавок (иначе называемых кондиломами остроконечными), напоминающих кочешки цветной капусты характерных образований, эпидермоплазии бородавчатой, папилломатоза ларингеального (типы 5, 17, 12, 6 и др.), могут исключительно редко при очень «благоприятных» условиях вызывать злокачественный процесс
- риска высокого, способные обуславливать у женщин неопластические изменения в области маточной шейки, папуллез бовеноидный (собственно ВПЧ 16 и 18 типа, 33, 31, 39, 35, 58, 56, 45, 68, 59, 52, 51), доказано провоцируют при наложении различных факторов онкологические процессы
Таким образом, ответ на вопрос о том, опасна ли ВПЧ 16 инфекция для здоровья женщины, определен: именно этот тип вируса несет серьезную угрозу.
Однако, присутствие возбудителя еще не означает наличие болезни.
К тому же, ВПЧ инфекция отличается интересной особенностью: способностью к самоизлечению.
Вот почему в ситуации, когда у женщин обнаружено при проведении лабораторных исследований некоторое количество ДНК ВПЧ 16 типа в анализах, важно не паниковать.
Просто нужно следовать рекомендациям врача и регулярно проходить обследование у гинеколога.
Результаты
В возрасте моложе 35 лет (включительно) были 79,8±4,4% пациенток группы наблюдения. Распределение инфицирования шейки матки 52, 58 и 59-м типами ВПЧ в зависимости от возраста было следующим: ранний репродуктивный возраст (18—25 лет) — 33 пациентки, средний (26—35 лет) — 34, старше 36 лет — 17.
Проведен анализ частоты ВПЧ-ассоциированных поражений шейки матки, которые подразделяют на клиническую (экзофитная кондилома), латентную (отсутствие клинических, морфологических изменений при обнаружении ДНК ВПЧ), субклиническую форму (невидимые невооруженным глазом, бессимптомные, выявляются только при кольпоскопии и/или морфологически), CIN I—III степени и РШМ [1]. Случаев клинической формы ПВИ не наблюдалось. Среди инфицированных женщин наблюдались пациентки с CIN (46—54,8%), относительно латентной формой инфекции без клинических ее проявлений (12—14,3%), субклинической формой инфекции (24—28,6%) и РШМ (2—2,4%).
В зависимости от тяжести гистологически верифицированного предрака CIN I установлена в 51,2%, CIN II — в 32,5%, CIN III — в 16,3% наблюдений.
При анализе частоты форм ПВИ, ассоциированной с изучаемыми типами в зависимости от возраста обращало внимание отсутствие существенных различий при латентной форме во всех возрастных группах (р
>0,05) (табл. 1). В свою очередь при наличии цервикальной патологии наглядно проявляется влияние возрастного фактора. Так, субклиническая форма ПВИ доминировала у пациенток раннего репродуктивного возраста по сравнению с таковой у пациенток 26—35 лет (
р
=0,05), у которых отмечено преобладание CIN (
р
=0,02). Не установлено существенных различий по степени тяжести CIN (I—III cтепени) в зависимости от возраста. Два случая РШМ, ассоциированного с 58-м типом ВПЧ, наблюдались в группе женщин старше 36 лет. Установлена прямая слабой силы, статистически значимая корреляция формы ПВИ и возраста (rS=+0,21;
p
=0,0517).
Таблица 1. Формы папилломавирусной инфекции, ассоциированной с 52, 58 и 59-м типами, в зависимости от возраста
При изучении характера инфицирования (моно-, сочетанное) установлено, что инфицирование шейки матки с участием одного из изучаемых типов ВПЧ наблюдалось у 37 (44%) пациенток: 52-й тип — у 19, 58-й тип — у 13, 59-й тип — у 5 (табл. 2). У 44 (52,4%) женщин наблюдалось сочетание с другими типами ВПЧ ВР 16, 18, 31, 33, 35, 39, 45, 51 и 56-м (наиболее часто встречались 16, 31 и 56-й типы), в трех случаях отмечено сочетание двух из 52, 58 и 59-го типов.
Таблица 2. Частота выявления ВПЧ 52, 58 и 59-го типов у женщин с ПВИ
Особое внимание было уделено моноинфекции изучаемых типов ВПЧ. Среди 37 женщин, у которых был выявлен один из типов (52, 58, 59-й), распределение форм заболевания было следующим: латентная — у 5 больных, субклиническая — у 12, CIN — у 19, рак — у 1. Цервикальная неоплазия (CIN и РШМ) составила при моноинфекции 20 (54%) случаев, при сочетанной форме — 28 (59,6%) случаев, что не имело статистически значимых различий (р
=0,3973). Частота CIN при моноинфекции 52-го типа — 6 наблюдений из 19 данного типа, при моноинфекции ВПЧ 58-го типа — 10 из 13, при моноинфекции ВПЧ 59-го типа — 3 из 5 наблюдений, РШМ (1 случай) — при моноинфекции ВПЧ 58-го типа (рис. 1).
Рис. 1. Распределение ВПЧ-ассоциированных поражений шейки матки при моно- и сочетанной формах инфекции.
Проведена оценка вирусной нагрузки ВПЧ 52, 58 и 59-го типов среди 84 инфицированных женщин (включая моно- и сочетанное инфицирование) (табл. 3). В 30 случаях ее уровень был ниже порога клинической значимости, в 30 случаях вирусная нагрузка ВПЧ 52, 58 и 59-го типов была в пределах от 3 до 5 lg на 105 клеток, в 33 случаях вирусная нагрузка была выше порога прогрессии. Превышение порога прогрессии варьировало в диапазоне 25—46,7% в зависимости от типа ВПЧ (рис. 2).
Таблица 3. Распределение уровня вирусной нагрузки по типам ВПЧ в группе обследованных пациенток (моно- и сочетанная инфекция) Примечание. * Здесь и в табл. 4: число наблюдений вирусной нагрузки не совпадало с числом обследованных пациенток в связи с сочетанным инфицированием.
Рис. 2. Вирусная нагрузка ВПЧ 52, 58 и 59-го типов у женщин с ПВИ.
При анализе взаимосвязи клинических форм ПВИ и уровня вирусной нагрузки установлено двукратное превышение случаев c нагрузкой, превышающей 5 lg на 105 клеток, у женщин с CIN: 25 против 10 (менее 3 lg на 105 клеток) и 11 (от 3 до 5 lg на 105 клеток) случаев, p
=0,0091 (табл. 4).
Таблица 4. Зависимость формы ПВИ при 52, 58 и 59-м типах ВПЧ (моно- и сочетанная инфекция) от вирусной нагрузки
В случае моноинфекции латентная форма не сопровождалась нагрузкой выше порога прогрессии, субклиническая форма протекала на фоне превышения порога прогрессии в 1 случае против остальных 11, в то время как ЦИН и РШМ — в 13 против 7 случаев с меньшей вирусной нагрузкой (табл. 5). Установлено наличие статистически значимой связи между тяжестью формы ПВИ и уровнем вирусной нагрузки 52, 58 и 59-го типов (2I=16,29; p
<0,05).
Таблица 5. Формы ПВИ при моноинфекции 52, 58 и 59-м типами ВПЧ
Согласно данным исследований, основанных на большом клиническом материале, среди различных возрастных групп повышение уровня вирусной нагрузки увеличивает тяжесть поражения шейки матки ВПЧ [5, 20, 22—24]. Согласно исследованию G. Shen и соавт. [25], отмечена положительная корреляция между уровнем вирусной нагрузки и степенью поражения шейки матки. Полученные нами данные доказывают влияние вирусной нагрузки для 52, 58 и 59-го типов ВПЧ на прогрессирование цервикальной неоплазии.
Откуда берется ВПЧ 16 типа у женщин
Согласно данным ВОЗ до 80% населения инфицировано ВПЧ.
Но только примерно 10% из инфицированных имеют клинические проявления.
Ответ на вопрос о том, как передается ВПЧ 16 женщинам, хорошо известен: основной путь заражения – сексуальный контакт.
В том числе и анально-генитальный и орально-генитальный, с инфицированным партнером.
У ВПЧ очень высокая распространенность: почти 80% женщин к 50-ти годам хотя бы раз инфицировались.
В то же время вирус имеет склонность к самоэлиминированию.
Так что установить вероятность заражения при однократном контакте не представляется возможным.
Вот почему так важно не пренебрегать профилактическими мероприятиями при случайных сексуальных актах.
Заражение ребенка матерью в момент рождения возможно вирусами 6 и 11 типа – причиной такого заболевания у детей, как респираторный папилломатоз.
Никакие другие типы вируса, в том числе ВПЧ 16 типа, при беременности, как правило, не вызывают проблем ни у женщин, ни у новорожденных.
Известны лишь единичные случаи заражения новорожденных матерями с бовеноидным папулезом.
Поэтому рутинное исследование на ВПЧ не рекомендовано ни одним международным/национальным руководством.
Инкубационный период варьируется от трех месяцев до нескольких лет.
Возможно одновременное заражение несколькими типами вирусов.
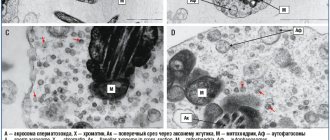
После проникновения в организм вирус поражает ткань, покрывающую поверхность тела и органы, ‑ эпителий, а именно его внутреннюю часть (базальный слой).
Вирус внутри клетки может не затрагивать хромосомы или встраиваться в геном.
Последний вариант, т.н. злокачественная форма, проявляется появлением клеток с измененной ДНК, которые размножаясь формируют опухоль.
Таким образом, если женщина – носитель ВПЧ 16 типа, 18, 6, 11 или иных, возможны следующие состояния:
- латентное течение инфекции, когда вирус не затрагивает клеточные ДНК, у женщин нет никаких клинических проявлений, а инфицирование обнаруживается только методом ПЦР
- появление таких клинических проявлений, как кондиломы, бородавки, папилломы, вирус при этом не изменяет клеточный геном, но провоцирует усиленное размножение клеток (проблема обнаруживается по наличии симптоматики, ПАП тесту, методом ПЦР)
- развитие неопластических изменений (дисплазии), когда вирус произвел изменение ДНК клетки и вызвал соответствующие изменения последней (такие изменения называются койлоцитозом), подтверждается ситуация ПЦР, ПАП-тестом, гистологическим и кольпоскопическим изучением
- карцинома, когда возбудитель изменил клеточный геном и вызвал образование большого числа измененных («атипичных») клеток – рака инвазионного (подтверждается диагноз ПЦР методом, ПАП-тестом, гистологическим и кольпоскопическим исследованиями)
В большинстве ситуаций (до 90%) на протяжении примерно 2 лет происходит самоизлечение организма от вируса.
Развитие же симптомов отмечается лишь у 1-5 % зараженных.
Что касается ВПЧ 16, причины возникновения серьезной клинической симптоматики у женщин включают:
- раннее начало половой жизни
- наличие множества секс-партнеров
- многократные беременности/роды до достижения возраста 20-ти лет
- курение
- хронический цервицит
- снижение иммунной защиты, например, из-за сопутствующей ВИЧ-инфекции (при функционировании нормальном иммунной системы рак у инфицированной женщины может развиться за 15-20 лет, тогда как у ВИЧ-инфицированной – за 5-10 лет, при этом ВИЧ увеличивает и вероятность заражения ВПЧ)
Распространенность
- 1Папилломавирусная инфекция является самой распространенной половой инфекцией.
- 2Среди сексуально активного населения инфицировано более 50%.
- 3Вероятность инфицирования вирусом папилломы человека увеличивается с ростом числа половых партнеров.
- 4Не генитальные кожные бородавки наиболее распространены среди подростков, а также взрослых, работающих с мясной продукцией (частота встречаемости – 10%).
- 5Папилломавирус чаще поражает женщин: вирус определяется у 22-35% женщин и 2-35% мужчин. Соотношение заболеваемости среди женщин и мужчин – 1.4:1.
- 6Онкогенные штаммы приводят к возникновению около 5% от всех раковых опухолей в мире.
Проявления ВПЧ-инфекции
В большинстве ситуаций при инфицировании ВПЧ в общем случае и, в частности, ВПЧ 16 симптомы у женщин, как и у лиц мужского пола, отсутствуют.
Иногда признаком инфекции могут служить бородавки, кондиломы (в случае присутствия вируса из группы низкого онкориска/неонкогенных).
При ВПЧ 16 заражении у женщин могут наблюдаться предраковые изменения на маточной шейке.
Это выявляется в процессе гинекологического осмотра.
Или профилактического, или, когда пациентка обратилась к врачу по иному поводу, например, с жалобами на необычные выделения.
Основными заболеваниями, вызываемыми ВПЧ 16, являются бовеноидный папулез и дисплазия разной степени.
При бовеноидном папулезе в области половых губ, лобка, паховой и околоанальной областях появляются плотные коричневатые, красноватые или телесного цвета папулы.
Они сливаются в крупные бородавчатые поверхности диаметром до 2 см.
Заболевание характеризуется хроническим, многолетним течением.
Озлокачествление развивается в 3% эпизодов (перерождается в плоскоклеточный рак), хотя чаще диагностируется самоизлечение.
Дисплазия маточной шейки относится к предраковым изменениям и требует серьезного отношения.
Поскольку такая патология из-за бессимптомности протекания может диагностироваться несвоевременно, в большинстве стран мира приняты программы скрининга рака цервикального.
Известно несколько классификационных подходов в отношении дисплазий и рака шейки.
Они основаны на результатах морфологических/цитологических изучений (исследований изменения клеток).
Согласно международной классификации болезней 10-го пересмотра различают:
- дисплазию легкую – незначительные разрастание и изменения эпителиальных клеток, часто подобное состояние обнаруживается при воспалительных процессах в области маточной шейки и устраняется после соответствующей противовоспалительной терапии
- дисплазию умеренную – изменения затрагивают весь нижний слой эпителия
- дисплазию тяжелую – поражается вся протяженность эпителия, заметно изменена структура клеток
- рак шейки (иначе карцинома плоскоклеточная) – обнаруживается при кольпоскопическом обследовании, подтверждается цитологически и гистологически
Умеренная и тяжелая дисплазия в большинстве эпизодов обусловлены именно воздействием вируса.
Признаки рака маточной шейки обнаруживаются лишь на последних стадиях и подразумевают:
- кровотечения межменструальные, нерегулярные, после полового контакта
- неприятный запах выделений
- дискомфорт во влагалище
- болевые ощущения с тазовой области, спине, ногах
- похудение
- утомляемость, отсутствие аппетита
- одностороннюю отечность ног
По мере прогрессирования болезни тяжесть проявлений может заметно нарастать.
Выводы
1. Среди когорты женщин с папилломавирусной инфекцией шейки матки, ассоциированной с 52, 58 и 59-м типами ВПЧ, значительная доля женщин моложе 35 лет (79,8%).
2. Установлен возрастзависимый характер частоты субклинической формы инфекции и цервикальной неоплазии у инфицированных женщин.
3. Папилломавирусная инфекция, ассоциированная с 52, 58 и 59-м типами ВПЧ, сопровождалась наличием CIN и рака шейки матки в 57,1% случаев.
4. Высокая частота цервикальной неоплазии при моноинфекции (54%), сопоставимая с ее частотой при сочетании с другими типами ВПЧ ВР (59,6%; р
>0,05), а также взаимосвязь тяжести поражения с уровнем вирусной нагрузки подтверждают высокий риск формирования предрака и рака шейки матки при наличии моноинфекции 52, 58 и 59-го типов ВПЧ.
Диагностика ВПЧ инфекции
Аногенитальные бородавки, причина которых вирусы 6 и 11 типа, легко обнаруживаются при гинекологическом осмотре.
Выявление таких образований является показанием для дополнительного осмотра маточной шейки, а при необходимости и уретры (уретроскопией).
Основным методом обнаружения неопластических изменений, обусловленных ВПЧ, является ПАП-тест.
Представляет собой цитологическое изучение мазков с маточной шейки.
В целом, онкоцитологией называют метод выявления раковых клеток в области шейки и влагалища.
Забор образцов материала для изучения осуществляется во время гинекологического осмотра специальными цито-щеточками и проходит абсолютно безболезненно.
Различают простую онкоцитологию, когда исследуемые клетки сразу наносятся на стеклышки для микроскопии.
И жидкостную, когда клетки предварительно обрабатываются специальным раствором и красителем.
К последнему типу и относится ПАП-тест.
После обработки материала двумя типами красителей в образце методом микроскопии легко обнаруживаются изменения клеточных ядер и цитоплазмы.
Предварительно определяют тип процесса патологии: воспалительный характер, злокачественный или др.
Затем по выраженности и характеру изменений проводят дифдиагностику возможных состояний.
ПАП-тест включен в скрининговую систему для выявления рака шейки матки во всех странах развитых.
Его ежегодное проведение показано всем лицам женского пола, достигшим возраста 20-ти лет.
К цитологическим признакам ВПЧ-инфекции относятся:
- койлоцитоз – появление характерных клеток-койлоцитов с объемными неровными ядрами, вакуолями (отсутствующими в норме) и зонами просветления около ядер
- дискератоцитоз – появление клеток-керацитов с темными ядрышками и характерно измененной цитоплазмой
Если ПАП-тест выявил изменение клеточных структур проводятся:
- кольпоскопическое изучение с уксуснокислым исследованием и тестом с раствором Люголя
- гистологическое исследование – под микроскопом изучаются небольшие фрагменты тканей (получают последние прицельной биопсией)
Кольпоскопические признаки инфекции:
- осветление обработанных уксусной кислотой участков
- окрашивание неравномерное раствором Люголя
- наличие характерных выростов (для низкоонкогенных типов вируса)
Согласно международным рекомендациям диагностическая тактика при выявлении нарушений методом ПАП-теста включает:
- Первый вариант – повтор обследования спустя три месяца, в случае нормы повтор через полгода и год, в случае аномалии – кольпоскопическое изучение
- Второй вариант – сразу проводится кольпоскопическое исследование, при не обнаружении аномальных отклонений повторяют цитологию спустя полгода (для онкогенных видов вируса). При необходимости проводят биопсию, выскабливание канала. В ситуации с недостаточной надежностью кольпоскопических данных рекомендуется противовоспалительная, эстрогеновая терапия с последующим повторением исследования
- Третий вариант – установление типа вируса методом гибридного захвата (т.н. дайджин-тестом, Digene) или ПЦР (полимеразной цепной реакцией). Обнаружение ВПЧ 16 типа или иного онкогенного вируса у женщин (норма – полное отсутствие возбудителя) служит показанием для кольпоскопии
Типирование папилломавирусов методом ПЦР имеет высокую диагностическую ценность с точки зрения определения типа вируса и его принадлежности к группе высокого риска онкологии.
Также для прогнозирования вероятности развития рака на фоне имеющихся неопластических изменений эпителия шейки матки.
Качественный анализ выдает результат в формате «есть вирус данного типа/нет».
Количественный метод (ПЦР в режиме «реального времени») позволяет обнаружить ДНК вируса даже в очень малых концентрациях от 10 – 100 копий в образце.
Может использоваться для отслеживания динамики развития инфекции.
По причине того, что у молодых женщин высок процент самоизлечения от ВПЧ, ПЦР рекомендуется для определения типа вируса лишь в возрасте после 30-ти лет.
Анализ крови с определением антител к ВПЧ не имеет диагностической ценности и проводится только с научно-исследовательскими целями.
Что же касается проблемы предпочтения Digene-теста или ПЦР, важно учитывать, что первый метод определяет у женщин количество ВПЧ 16 типа и других типов) от 5000 копий.
Тогда как ПЦР «чувствует» значительно меньшее содержание.
Этот момент существенен с той точки зрения, что именно такое число является клинически значимым.
Т.е. обнаружено более 5000 копий на фоне неопластических состояний – высок риск онкологии.
А обнаружение меньшего количества не позволяет прогнозировать риск развития рака на фоне дисплазии.
В общем случае данные анализа позволяют врачу решить, стоит ли начать лечение или ограничиться наблюдением.
Скрининг и лечение предраковых поражений шейки матки
Скрининг
Скрининг на рак шейки матки включает тестирование на ВПЧ-инфекцию для выявления предраковых состояний с последующим назначением соответствующего лечения. Тестирование проводится среди женщин, не имеющих симптомов и чувствующих себя совершенно здоровыми. Если скрининг выявляет ВПЧ-инфекцию или предраковые поражения, их можно легко лечить и тем самым предотвратить развитие рака. Скрининг может также выявить рак на ранней стадии, когда существует высокая вероятность излечения.
В настоящее время в обновленном руководстве ВОЗ странам рекомендуется использовать для цервикального скрининга тесты на ВПЧ, в частности:
- тесты на ДНК ВПЧ, позволяющие выявлять высокоопасные штаммы ВПЧ, вызывающие почти все виды рака шейки матки;
- тесты на мРНК ВПЧ, позволяющие выявлять ВПЧ-инфекции, приводящие к появлению атипичных клеток.
Тесты на ВПЧ, в отличие от визуального обследования, позволяют получить объективный результат. Они зарекомендовали себя простотой использования, возможностью выявления большего числа предраковых и раковых состояний и спасения большего числа жизней. Их применение также более экономически оправдано по сравнению с визуальными методами обследования или цитологией (мазок Папаниколау).
В общей популяции женщин скрининг должен проводиться с использованием валидированного теста на ВПЧ начиная с 30-летнего возраста с интервалом каждые 5–10 лет; среди женщин с ВИЧ-инфекцией его следует проводить начиная с 25-летнего возраста. Кроме того, скрининг среди ВИЧ‑инфицированных женщин должен проводиться чаще, каждые 3–5 лет.
Для проведения цитологии и теста на ВПЧ медицинским персоналом применяются аналогичные процедуры взятия цервикального образца. ВОЗ допускает возможность самостоятельного взятия образцов пациенткой при проведении теста на ДНК (но не мРНК) ВПЧ. Для уверенного выполнения данной процедуры женщинам должна оказываться надлежащая поддержка.
Скрининг должен быть увязан с лечением и ведением пациентов с положительными результатами скрининга. ВИЧ-положительным женщинам в условиях нехватки ресурсов лечение может назначаться без подтверждающей диагностики. При этом лечение ВИЧ-положительных женщин можно начинать только после получения положительного на ВПЧ результата теста (например, визуального обследования с использованием уксусной кислоты).
Лечение предраковых положений
В случае необходимости лечения предраковых поражений и соответствия пациентки критериям лечения рекомендуется проводить удаление пораженных тканей методом криотерапии или термоабляции. Оба метода лечения эффективны и безопасны и могут выполняться в амбулаторных условиях.
В случае несоответствия критериям аблятивного лечения или при наличии подозрений на рак шейки матки пациентку необходимо направить в специализированное медицинское учреждение, в котором имеются возможности для проведения надлежащего обследования методами кольпоскопии и биопсии. При необходимости ей может быть назначена эксцизия (LLETZ), а в случае рака – составлен индивидуальный план лечения с учетом стадии заболевания, состояния здоровья и предпочтений пациентки, а также доступности медицинских ресурсов.
Лечение ВПЧ инфекции
Какой врач лечит ВПЧ 16 у женщин?
Лечением ВПЧ-инфекции может заниматься врач-гинеколог, онколог, инфекционист, венеролог.
Важно понимать, что случайное обнаружение вируса при отсутствии клинических изменений не является показанием для проведения терапии.
Только в случае выявления высокоонкогенных вирусов (ВПЧ 16) у женщин врач решает, что делать дальше.
Нужно ли участить прохождение диагностических обследований и осмотров или назначить дополнительные исследования.
Только специалист может установить, нужно ли лечить ВПЧ 16 у женщин, учитывая наличие/отсутствие индуцированных вирусом изменений.
В ситуации с ВПЧ важно доверять свое здоровье только высокопрофессиональным специалистам, знакомым с международными протоколами ведения инфекции.
Особенно это существенно при инфицировании ВПЧ 16, провоцирующего злокачественные патологии у женщин (отзывы в интернете, от знакомых помогут определиться с учреждением и врачом).
На сегодняшний день у женщин лечение ВПЧ 16 основано на удалении атипически измененного эпителия.
Следует понимать, что при наличии инфекции у женщин препараты, уничтожающие сам вирус, отсутствуют на сегодняшний день.
Любая международная схема лечения ВПЧ 16 не предусматривает включение каких-либо противовирусных средств.
В то же время проводится специфическое лечение ВПЧ 16, при котором рекомендуются к приему у женщин препараты с иммуномодулирующей и противовирусной активностью.
Считается, что такие средства мобилизуют иммунитет на предмет борьбы с вирусом.
Подобные средства не прошли достаточной проверки эффективности клиническими испытаниями.
Соответственно, нет достоверных данных о проценте излеченности.
Несмотря на это, многие пациенты отмечают существенное улучшение самочувствия на фоне их использования.
К средствам иммунокорригирующей терапии от ВПЧ 16 у женщин относят:
- с человеческим рекомбинантным интерфероном или его индукторами свечи (Виферон, Генферон), Изопринозин, Циклоферон и др.
- с иммуностимулирующим эффектом ‑ Ликопид, Полиоксидоний и пр.
- витамины группы В, омега-кислоты и БАДы
Зачастую перед назначением медикаментозной схемы лечения рекомендуется проведение анализа иммунного статуса (иммунограммы).
С определением показателей активности моноцитов, нейтрофилов, функции лимфоцитов, уровней иммуноглобулинов, CD16+, CD8+, CD4+ и других.
К сожалению, для многих препаратов не получены данные по безопасности применения, осложнениям и рецидивам после использования.
Поэтому рекомендуется воздержаться от их применения лицам с:
- аутоиммунными заболеваниями
- злокачественными образованиями (при раке шейки матки могут назначаться только после завершения хирургического лечения)
- аллергическими реакциями
- бронхиальной астмой и др.
Что касается общепринятого в международном медицинском сообществе подхода к ведению ВПЧ-инфекции, то здесь позиционируются следующие моменты:
- Не существует лекарственных средств для удаления вируса из организма, но при этом вероятность самоизлечения очень высока, особенно в молодом возрасте
- При отсутствии изменений клеточных структур и выявлении вируса из группы высокого онкогенного риска проводится более частое и тщательное наблюдение за пациенткой
- При обнаружении изменений, вызванных активностью вируса, проводится терапия, направленная на устранение патологических преобразований
При бовеноидном папулезе, обусловленном ВПЧ 16 типа, проводят удаление образований методами:
- иссечения по Мохсу
- лазерной терапии
- криодеструкции
- электрокоагуляции
- местным наложением мазей с цитостатиками (5-фторуроциловой, проспидиновой, фторофуровой)
- внутриочаговым введением интерферона
- приема внутрь капсул Неотигазона
Предраковые состояния и первые стадии рака маточной шейки хорошо поддаются лечению.
Измененные клетки удаляют методом криотерапии.
При дисплазиях проводятся органосохраняющие операции: конизация шейки скальпелем, электрохирургически, лазером с предварительным канальным выскабливанием.
При локализованных формах опухоли проводят хирургическое лечение, при распространенном процессе – лучевая и химиотерапии.
С учетом того, что устранение результата активности вируса не удаляет сам возбудитель инфекции.
Риск рецидива патологических изменений остается, что, в свою очередь, требует дальнейшего наблюдения за пациенткой.
Кроме того, нельзя исключить и вероятность реинфицирования ВПЧ.
После реализации любого варианта лечения рекомендуется проведение контрольных анализов.
Поскольку существует вероятность самопроизвольного устранения вируса в течение 2-х лет от момента заражения.
Отдельную проблему представляют лица с ВПЧ на фоне ВИЧ-инфицирования.
Доказано, что риск развития онкологии у таких женщин выше, как и риск собственно заражения ВПЧ.
Хотя чаще выявлялось первичное инфицирование ВПЧ, что связано с большей распространенностью этого вируса.
Причем чем хуже иммунный статус пациентки, тем выше вероятность возникновения у нее ВПЧ-индуцированного рака.
Поэтому лицам с ВИЧ-статусом рекомендуется более частое прохождение исследований на ВПЧ.
Лечение проводится теми же методами, что и у неинфицированных ВИЧ, с проведением дополнительно специфической терапии, направленной на подавление активности вируса иммунодефицита.
Каковы последствия ВПЧ при беременности?
На сегодняшний день нет достоверных доказательств выраженного негативного воздействия инфекции на течение беременности.
Такие характерные для иных половых инфекций патологии беременности, как невынашивание, преждевременные роды и т. п., не нашли безусловного подтверждения связи с ВПЧ.
Тем не менее, если первичное инфицирование женщины произошло именно в период беременности, риск развития различных осложнений присутствует.
Некоторые последствия для плода при беременности имеют аногенитальные бородавки у матери, вызванные ВПЧ 6 и 11 типа, с локализацией в области малых половых губ и преддверия влагалища.
Такие остроконечные кондиломы несут небольшой риск заражения плода в родах, приводя к развитию у последнего респираторного папилломатоза.
Респираторный, или иначе ларингеальный, папилломатоз (также называемый папилломатозом гортани) чаще всего развивается у детей 2-х – 3-х лет.
В результате заражения от больной матери еще в период беременности последней или непосредственно при рождении.
Путь передачи во время беременности через плаценту, в ходе родов или непосредственно после них, пока не вполне ясен.
Основными симптомами заболевания являются осиплость, вплоть до полного исчезновения голоса, и затруднения глотания.
По мере прогрессирования болезни появляются отдышка, кашель.
В тяжелых ситуациях возможно перекрывание верхних дыхательных путей, асфиксия, особенно в случае образований с длинной тонкой ножкой.
В процессе осмотра посредством ларингоскопа (иногда применяется и бронхоскоп) на слизистой гортани обнаруживаются типичные разрастания – кондиломы.
Такая патология отличается довольно агрессивным течением: после удаления образований часто происходят рецидивы, требующие повторных хирургических вмешательств.
Если наступает беременность при инфицировании папилломавирусами высокой онкогенности (особенно ВПЧ 16, 18), женщина должна обязательно сообщить о наличии инфекции своему акушеру-гинекологу.
Дело в том, что изменения в организме беременной женщины могут спровоцировать более интенсивное преобразование клеток.
Собственно, на течение самой беременности, на ребенка такие вирусы не оказывают влияния, но создают определенную угрозу здоровью женщины.
В ситуации, когда инфекции в прошлом выявлено не было, при постановке на учет среди прочих берется и цитологический мазок по Папаниколау (ПАП-тест).
Если анализ показывает отклонения, то врач назначает дополнительные исследования (например, кольпоскопию).
Также особого внимания требуют ситуации, когда беременность наступает у женщин с эрозией.
Обязательно проводится ПЦР-диагностика для исключения инфицирования ВПЧ высокого онкогенного риска.
Как правило, в рутинной практике акушера-гинеколога специально не исследуется такое сочетание, как ВПЧ и беременность.
Анализы на вирус рекомендуются только при обнаружении патологических отклонений.
В то же время существуют исследовательские работы, демонстрирующие влияние вируса на наступление беременности.
Так, было показано, что инфицирование женщин ВПЧ несколько снижает вероятность приживания эмбриона, а у мужчин уменьшает подвижность сперматозоидов.
А поскольку в семейной паре, как правило, инфицированными оказываются оба партнера, то наступление беременности сопряжено с некоторыми трудностями.
В результате при планировании беременности на фоне инфекции, вызванной ВПЧ, планировании процедуры ЭКО следует учитывать и этот фактор.
Диагностические мероприятия
Раннее выявление факта заражения ВПЧ 16 типа возможно только с использованием молекулярной диагностики.
Она позволяет установить уникальные последовательности ДНК, присущие только искомым папилломавирусам.
Для этого используется три вида методик:
- неамплификационные
- амплификационнные (ПЦР)
- сигнальные амплификационные (система гибридной ловушки – Digene Hybrid Capture System II)
Анализы первого типа в практической медицине не используются из-за высокой стоимости и сложности постановки.
Амплификационные методы, среди которых наиболее изучена ПЦР, применяются достаточно широко и хорошо изучены.
Позволяют установить факт заражения именно ВПЧ 16.
Выявляют вирусы других типов (заразиться несколькими представителями папилломмавирусов одновременно вполне реально).
Методика ПЦР в реальном времени еще и устанавливает концентрацию ДНК онкогенных вирусов.
Такой показатель имеет важно прогностическое значение в динамике.
Изначально большие цифры на начало лечения должны постепенно падать под влиянием специальной терапии.
И полностью исчезнуть после любого деструктивного лечения, хирургического вмешательства.
Если же концентрация вирусной ДНК в диагностическом материале изначально невысока, то врач может порекомендовать выжидательную тактику.
Иногда есть 20% вероятность, что ВПЧ 16 типа с низкой концентрацией ДНК самопроизвольно элиминируется из очага.
Digene (или Дайджин-тест) от ПЦР отличаются беспрецедентной точностью и высокой скоростью проведения исследования (в течение одного дня).
Также Дайджин позволяет провести количественный анализ (подсчитать концентрацию) вирусной ДНК.
От внедрения этой методики в широкую клиническую практику удерживает только заметная стоимость исследований.
Для проведения таких достаточно сложных и высокотехнологических анализов, мужчине следует обращаться к врачам, имеющим доступ к современным лабораторным центрам.
Применение онкоцитологии, – самого известного способа диагностики опухолевых процессов, является оправданным только для выработки тактики лечения мужчины.
Метод позволяет установить, состоялось ли перерождение клеток образования в злокачественный процесс или папиллома еще остается доброкачественной.
Эта информация, предоставляемая онкоцитологическим исследованием образца тканей из подозрительного очага, является определяющей для разработки тактики лечения.
Иммунограмма в классическом ее понятии, для диагностики ВПЧ инфекции 16 типа у мужчин представляет небольшую ценность.
С ее помощью можно только установить примерный срок заражения – по типам выявленных иммуноглобулинов.
IgA и IgM обнаруживаются при недавнем инфицировании, а IgG – когда давность заражения составляет несколько месяцев.
Лечебные мероприятия
Учитывая высокий риск развития злокачественной опухоли на месте поражения ВПЧ 16, лечить нужно всех мужчин с подтвержденным диагнозом.
Независимо от концентрации возбудителей.
Особенно, если образование достаточно крупное и/или расположено в области уретры, мешает мочиться.
Исключение – когда при небольших папилломах обнаруживаются малые концентрации вирусной ДНК.
Это дает определенный шанс на самостоятельное выздоровление.
Притом необходимо обеспечить регулярный контроль за состоянием папилломы.
Но и здесь, по индивидуальным показаниям, врач может рекомендовать все-таки пролечиться.
Общих подходов три:
- удаление внешних проявлений инфекции – вместе с пораженными клетками убираются и вирусы
- консервативное лечение – применение разного вида лекарств и препаратов, как местного действия, так и системного
- комбинированный подход – сбалансированное сочетание хирургической и консервативной составляющей
Как правило, наилучший эффект достигается при использовании третьего подхода.
Поэтому мужчине лучшее сразу настроиться, что лечиться придется минимум в двух учреждениях.
Хирургического профиля для этапа удаления папилломы и терапевтического – для закрепления достигнутых результатов.
Также необходимо будет периодически обследоваться, чтоб убедиться в эффективности лечения или обнаружить ранние признаки рецидива.
Все – в амбулаторном режиме, без лишних затрат времени и денег.